
【题目】化合物F是一种调香剂,结构为![]() ;以化合物A为原料合成F的工艺流程如图:
;以化合物A为原料合成F的工艺流程如图:

根据上述信息回答下列问题:
⑴化合物A的名称___,化合物E中含氧官能团的名称是___。
⑵①反应类型是___,反应②的反应试剂是___。
⑶D的结构简式是___。
⑷E的顺式异构体的结构简式___。
⑸反应⑤的化学方程式是___。
⑹F在一定条件下能发生加聚反应,其加聚反应的产物的结构简式是___。
【答案】2-甲基-1-丁烯 羧基 加成反应 NaOH溶液 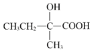
![]()
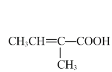 + CH3CH2OH
+ CH3CH2OH![]() H2O +
H2O + ![]()
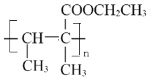
【解析】
A(![]() )和氯气发生加成反应生成B,B发生水解反应生成C(
)和氯气发生加成反应生成B,B发生水解反应生成C(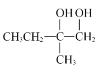 ),C选择性氧化反应生成羧酸D(
),C选择性氧化反应生成羧酸D( ),
), 发生消去反应生成E,E和乙醇发生酯化反应生成F(
发生消去反应生成E,E和乙醇发生酯化反应生成F(![]() )。
)。
⑴化合物A![]() ,其名称为2-甲基-1-丁烯,化合物E(
,其名称为2-甲基-1-丁烯,化合物E( )中含氧官能团的名称是羧基;故答案为:2-甲基-1-丁烯;羧基。
)中含氧官能团的名称是羧基;故答案为:2-甲基-1-丁烯;羧基。
⑵根据前后分析得到①反应类型是加成反应,反应②是水解反应,其反应试剂是NaOH溶液;故答案为:加成反应;NaOH溶液。
⑶C到D是选择性氧化,只氧化后面的羟基,因此D的结构简式是 ;故答案为:
;故答案为: 。
。
⑷E的顺式异构体的结构简式![]() ;故答案为:
;故答案为:![]() 。
。
⑸反应⑤是发生酯化反应,其化学方程式是 + CH3CH2OH
+ CH3CH2OH![]() H2O +
H2O + ![]() ;故答案为:
;故答案为: + CH3CH2OH
+ CH3CH2OH![]() H
H![]() 。
。
⑹F在一定条件下能发生加聚反应,其加聚反应的产物的结构简式是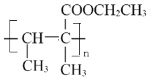 ;故答案为:
;故答案为: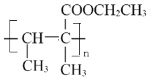 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知热化学方程式![]() O2(g) +C2H2(g) =2 CO2(g) + H2O (g) ΔH = -1256 kJ·mol-1,下列正确的是( )
O2(g) +C2H2(g) =2 CO2(g) + H2O (g) ΔH = -1256 kJ·mol-1,下列正确的是( )
A.乙炔的燃烧热为1256 kJ·mol-1
B.若生成2 mol液态水,则ΔH = -2512 kJ·mol-1
C.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ
D.若转移10 mol电子,则消耗2.5 mol O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁钢轨全部为无缝钢轨,钢轨焊接可以采用铝热法,其原理如图所示。下列叙述错误的是( )

A.铝热法炼铁的原理是
B.该实验需要关注的安全事项之一是纸漏斗与盛沙子的蒸发皿的距离不要太远,否则熔融的铁水易溅出伤人
C.点燃镁条,镁条剧烈燃烧,放出大量的热,使氧化铁粉末和铝粉在较高的温度下发生剧烈的反应
D.![]() 和
和![]() 的质量比要控制在
的质量比要控制在![]() ,且要混合均匀,以保证
,且要混合均匀,以保证![]() 和
和![]() 都能完全反应
都能完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在密闭容器中,反应aA(g)![]() bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新平衡时,A物质的量浓度变为原来的60%,则ab(填“>、=、<”),简述其理由。
bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新平衡时,A物质的量浓度变为原来的60%,则ab(填“>、=、<”),简述其理由。
(2)在恒温时,在固定容器中充入N2O4,发生反应N2O4(g)![]() 2NO2(g),在达到平衡后,若又向容器中充入一定量的N2O4,当达到新平衡时,反应体系中NO2(g)的体积分数将(增大、减小、不变)。
2NO2(g),在达到平衡后,若又向容器中充入一定量的N2O4,当达到新平衡时,反应体系中NO2(g)的体积分数将(增大、减小、不变)。
(3)在一定体积的密闭容器中,进行反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其反应化学平衡常数和T的关系如下表所示:
CO(g)+H2O(g),其反应化学平衡常数和T的关系如下表所示:
T/℃ | 700 | 800 | 830 | 1000 | 1200[来 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
A.对于CO(g)+H2O(g)![]() CO2(g)+H2(g)此平衡体系,升温平衡向移动。
CO2(g)+H2(g)此平衡体系,升温平衡向移动。
B.达到平衡后,若压缩容器的体积,正逆反应速率的变化是。
C.对原平衡,在t0时升高温度对化学反应速率产生影响,请在下图中绘出速率变化图:
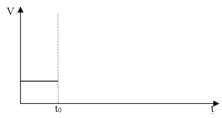
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KA1(SO4)2·12H2O]是一种复盐,在造纸等方面应用广泛。采用废易拉罐制备明矾的过程如下图所示。
下列叙述错误的是

A. 合理处理易拉罐有利于环境保护和资源再利用
B. 从易拉罐中可回收的金属元素有Al、Fe
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用NaHSO4代替NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为:CO(g)+2H2(g)= CH3OH(g),在体积为1L的恒容密闭容器中,充入2 molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始至达到平衡,用氢气表示的平均反应速率υ(H2)=_______mol/(L·min)
②下列说法正确的是______(填字母序号)。
A.达到平衡时,CO的转化率为75%
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充入氩气,反应速率减小
D.2min前υ(正)>υ(逆),2min后υ(正)<υ(逆)
③该条件下反应的平衡常数K=______。
(2)已知:I.CO的燃烧热为△H=-283.0kJ·mol-1
II.H2O(1)=H2O (g) △H=+44.0 kJ·mol-1
III.2CH3OH(g)+CO2(g)![]() CH3OCOOCH3(g)+ H2O(g) △H=-15.5 kJ·mol-1
CH3OCOOCH3(g)+ H2O(g) △H=-15.5 kJ·mol-1
则①2CH3OH(g)+CO(g)+![]() O2(g)
O2(g)![]() CH3OCOOCH3(g)+ H2O( l) △H=_____。
CH3OCOOCH3(g)+ H2O( l) △H=_____。
②对于可逆反应2CH3OH(g)+CO(g)+ ![]() O2(g)
O2(g)![]() CH3 OCOOCH3(g)+H2O(1)采取以下措施可以提高CH3OCOOCH3产率的是____(填字母)
CH3 OCOOCH3(g)+H2O(1)采取以下措施可以提高CH3OCOOCH3产率的是____(填字母)
A.降低体系的温度 B.压缩容器的体积
C.减少水量 D.选用适当的催化剂
(3)比亚迪双模电动汽车使用高铁电池供电。高铁电池的总反应为:3Zn(OH)+2Fe(OH)3+4KOH![]() 3Zn+2K2 FeO4+8H2O,则充电时的阳极反应式为_______。
3Zn+2K2 FeO4+8H2O,则充电时的阳极反应式为_______。
(4)若往20mL0.0lmol/L的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如下图所示,下列有关说法正确的是______(填序号)。

①该烧碱溶液的浓度为0.02mol/L
②该烧碱溶液的浓度为0.01mol/L
③HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:K3[Fe(CN)6]溶液是检验Fe2+的试剂,若溶液中存在Fe2+,将产生蓝色沉淀。将0.1mol/L的KI溶液和0.05mol/L Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“”2Fe3++2I-![]() 2Fe2++I2的是
2Fe2++I2的是
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A.①和③B.②和④C.③和④D.①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
2 H2(g)+ O2(g)= 2H2O(g)△H2
C(s)+ O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H为
A. 12△H3+5△H2-2△H1 B. 2△H1-5△H2-12△H3
C. 12△H3-5△H2-2△H1 D. △H1-5△H2-12△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
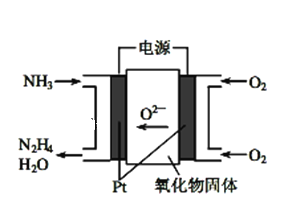
【题目】(1)工业上利用N2和H2合成NH3,NH3又可以进一步制备联氨(N2H4)等。由NH3制备N2H4的常用方法是NaClO氧化法,其离子反应方程式为______________________,有学者探究用电解法制备的效率,装置如图,试写出其阳极电极反应_________________________;
(2)乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇(CH3CH2OH)的一种反应原理为:2CO(g)+4H2(g) ![]() CH3CH2OH(g)+H2O(g) △H=-akJ/mol,己知:CO(g)+H2O(g)
CH3CH2OH(g)+H2O(g) △H=-akJ/mol,己知:CO(g)+H2O(g) ![]() CO2(g)+H2(g) △H=-bkJ/mol,以CO2(g)与H2(g)为原料也可合成气态乙醇及水蒸气,并放出热量,写出该反应的热化学反应方程式: _______________________________。
CO2(g)+H2(g) △H=-bkJ/mol,以CO2(g)与H2(g)为原料也可合成气态乙醇及水蒸气,并放出热量,写出该反应的热化学反应方程式: _______________________________。
(3)如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
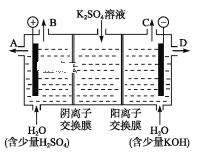
①该电解槽的阳极反应为_______________。 此时通过阴离子交换膜的离子数_____(填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)_______导出。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com