
危险化学药品的包装标签上印有警示标志。下列化学药品名称与警示标志对应正确的是
A.汽油—易燃品 B.浓硫酸—易爆品
C.酒精—剧毒剂 D.浓硝酸—三级放射性物品
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源:2014-2015学年吉林公主岭市高一上学期第一次月考化学试卷(解析版) 题型:选择题
用NA表示阿伏伽德罗常数,下列叙述正确的是( )
A.64gSO2含有氧原子数为1NA
B.物质的量浓度为0.5mol/L的MgCl2溶液,含有Cl-数为1NA
C.标准状况下,22.4LH2O的分子数为1NA
D.常温常压下,14gN2含有分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高二上第一次质量检测化学试卷(解析版) 题型:选择题
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是
C(s)+ 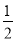 O2(g)=CO(g) △H=―393.5kJ/mol
O2(g)=CO(g) △H=―393.5kJ/mol
B.2H2(g)+O2(g)=2H2O(l) △H=+571.6kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=―890.3kJ/mol
D.C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) △H=―2800kJ/mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:选择题
下列实验操作正确的是
编号 | 实验 | 操作 |
A | 实验室用自来水制备蒸馏水 | 将自来水倒入烧杯中,小心给烧杯加热 |
B | 配制一定浓度的氯化钾溶液100mL | 将称好的氯化钾固体放入100 mL容量瓶中,加水溶解,振荡摇匀,定容 |
C | 除去粗盐溶液中的Ca2+、SO42- | 依次加入过量的BaCl2溶液、Na2CO3溶液,过滤后再加适量盐酸 |
D | 取出分液漏斗中的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:选择题
下列分散系中的分散质的微粒直径属于纳米级(1~100nm)的是( )
A.溶液 B.悬浊液 C.乳浊液 D.胶体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高二上学期期中考试化学试卷(解析版) 题型:填空题
(8分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5 mol·L-1盐酸、0.55 mol·L-1NaOH溶液,实验尚缺少的玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
(3)他们记录的实验数据如下:
实验用品 | 溶液温度 | 中和热 | ||||
T1 | t2 | ΔH | ||||
① | 50 mL0.55 mol·L-1 NaOH溶液 | 50 mL0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.3 ℃ |
| |
② | 50 mL0.55 mol·L-1 NaOH溶液 | 50 mL0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.5 ℃ | ||
(已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。)
根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用KOH代替NaOH,对测定结果 (填“有”或 “无”)影响;若用醋酸代替HCl做实验,对测定结果 (填“有”或“无”)影响。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高二上学期期中考试化学试卷(解析版) 题型:选择题
某温度下在密闭容器中发生如下反应3 M(g)+ N(g) 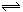 2G(g)
2G(g)
若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入3 molM和1molN的混合气体,达平衡时M的转化率为
A.20% B.40% C.60% D. 80%
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高二上学期期中考试化学试卷(解析版) 题型:选择题
下列关于平衡常数K的说法中,正确的是
A.在任何条件下,化学平衡常数是一个恒定值
B.改变反应物浓度或生成物浓度都会改变平衡常数K
C.平衡常数K只与温度有关,与反应浓度、压强无关
D.从平衡常数K的大小不能推断一个反应进行的程度
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区八校高二上学期期中联考化学试卷(解析版) 题型:填空题
粉末状试样A是由等物质的量的MgO和Fe2O?组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20克A全部溶于0. 15L 6mol·L -1的盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12L气体(标准状况),同时生成溶液D,还有残留固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请填空:
(1)①中引发铝热反应的实验操作是 ,
产物中的单质B是 。
(2)②中所发生的各反应的化学方程式是 、 。
(3)③中所发生的各反应的离子方程式是 、 。
(4)若溶液D的体积仍视为0.15L,则该溶液中c(Mg2+)为 ,c(Fe2+)为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com