
【题目】下列关于化合物、单质、混合物、电解质和非电解质的正确组合是( )
化合物 | 单质 | 混合物 | 电解质 | 非电解质 | |
A | 烧碱 | 液态氧 | 冰水混合物 | 醋酸 | 二氧化硫 |
B | 生石灰 | 白磷 | 胆矾 | 氧化铝 | 氯气 |
C | 干冰 | 铁 | 氨水 | 石灰石 | 酒精 |
D | 空气 | 氮气 | 小苏打 | 氯化铜 | 硫酸钡 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%.现取20mL pH=3的 CH3COOH溶液,加入0.2molL﹣1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( ) 
A.0.5%
B.1.5%
C.0.1%
D.1%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是制取无水氯化铁的实验装置图。请回答下列问题:
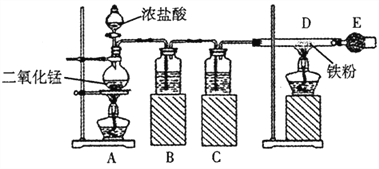
已知:氯化铁易潮解。
(1)烧瓶中发生反应的化学方程式是_________________;
(2)B瓶中的溶液是_________________,C瓶中溶液的作用是_________________。
(3)干燥管E中盛有碱石灰,其作用是_________________。
(4)开始实验时,应先点燃_________________(填字母)处的酒精灯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是( )
A.Na+、Mg2+、OH-、Br-B.H+、Fe2+、SO42-、NO3-
C.K+、NH4+、CO32-、OH-D.Ca2+、Al3+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为;
(2)反应是反应.(选填“吸热”、放热).
(3)能判断该反应是否达到化学平衡状态的依据是 .
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)c(CH2)=c(CO)c(H2O),试判断此时的温度为℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本类型反应的关系如右图所示,则下列化学反应属于氧化还原反应但不包含在1,2,4范围内的是( )

A. Cl2+2KBr=Br2+2KCl B. 2NaHCO3![]() Na2CO3+H2O+CO2
Na2CO3+H2O+CO2
C. 4Fe(OH)2+O2+2H2O=4Fe(OH)3 D. 2Na2O2+2CO2=2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,工业上由铬铁矿(主要成分为FeOCr2O3、SiO2等)制备,制备流程如图所示:

已知:a.步骤①的主要反应为: 2FeOCr2O3+4Na2CO3+ 7NaNO3 ![]() 4Na2CrO4+Fe2O3+4CO2+7NaNO2 b. 2CrO42-+2H+
4Na2CrO4+Fe2O3+4CO2+7NaNO2 b. 2CrO42-+2H+ ![]() Cr2O72-+H2O
Cr2O72-+H2O
下列说法正确的是
A. 步骤①熔融、氧化可以在陶瓷容器中进行
B. 步骤①中每生成44.8L(标况下) CO2共转移14mol电子
C. 步骤④若调节滤液2的pH使之变大,则有利于生成Cr2O72-
D. 步骤⑤生成K2Cr2O7晶体,说明该温度下K2Cr2O7溶解度小于Na2Cr2O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2分别通入下列4种溶液中,有关说法不正确的是( )
A. 试管a中实验可以证明SO2具有还原性 B. 试管b中溶液褪色,说明SO2具有漂白性
C. 试管c中能产生白色沉淀,说明SO2具有氧化性 D. 试管d中能产生白色沉淀,该沉淀不溶于稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式______。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式______。
(3)酸雨是指pH<_____的降水。大量燃烧含硫煤产生气体随雨水降落到地面,随时间变长雨水酸性会逐渐增强,试用化学方程式解释其原因_________。在煤中加入适量石灰石,可以大大减少煤燃烧时SO2的排放,同时得到硫酸钙,发生反应的化学方程式__________。
(4)空气质量报告的各项指标可以反映出各地空气的质量,下列气体已纳入我国空气质量报告的是______(填字母)。
A.CO2 B.N2 C.NO2 D.O2
(5)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与金属铜发生反应的离子方程式___________。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是_______。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com