
从海带中提取碘,有甲、乙两种实验方案如下:
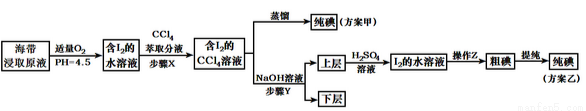
已知:3I2+6NaOH=5NaI+NaIO3+3H2O。请回答:
(1)步骤X使用分液漏斗前须检漏,检漏方法为_________。
(2)用右图所示装置进行蒸馏。指出右图所示实验装置中的任意两处错误:
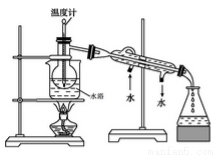
①___________;②__________。
(3)进行上述操作时,使用水浴加热更好的原因是___________;最后碘晶体在__________里聚集。
(4)下列有关步骤Y的说法,正确的是________。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
(5)方案乙在上层溶液中加入H2SO4溶液得到I2的水溶液发生的反应方程式是:_____________;
(6)操作Z的名称是____________。
(7)工业中采用方案乙从海带中提取碘,方案甲中采用蒸馏不合理,理由是______________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年湖南省高二上月考三化学卷(解析版) 题型:选择题
化学与STSE(社会、科学、技术和环境)密切相关,下列说法正确的是
①寻找合适催化剂提高合成氨工业中原料的转化率
②氟氯烃分解产生的氯原子因能降低臭氧分解的活化能而加速臭氧的分解反应
③氟化物防止龋齿所涉及到的化学原理其实就是沉淀的转化
④煤气中毒或救治与氧气、一氧化碳和血红蛋白结合过程中的化学平衡移动有关
A.①②③ B.②③④ C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江牡丹江第一高级中学高三12月月考化学卷(解析版) 题型:选择题
下列叙述正确的是
①硫酸钡难溶于水和酸,可做X光透视肠胃的药剂
②神舟10号飞船所用太阳能电池板的材料是单晶硅
③医用酒精是利用了乙醇的氧化性来杀菌消毒的
④玛瑙饰品的主要成分与建筑材料砂子不相同
⑤碳酸钠、氢氧化钠、碳酸钙、碳酸氢钠等都可以中和酸,故都可以作为治疗胃酸过多的药物
⑥明矾净水利用了胶体的性质
⑦根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸
⑧金属钠具有强的还原性,可利用钠和熔融TiCl4反应制取金属Ti
A.①②③⑦ B.①②⑥⑧ C.①③④⑧ D. ①③⑥⑦
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江哈尔滨三中高三上验收考试三化学卷(解析版) 题型:选择题
市场上经常见到的一种电池,总反应式为:Li+2Li0.35NiO2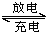 2Li0.85NiO2。负极材料是金属锂和碳的复合材料,含Li+导电固体为电解质,下列说法正确的是
2Li0.85NiO2。负极材料是金属锂和碳的复合材料,含Li+导电固体为电解质,下列说法正确的是
A.放电过程中Li+向正极移动
B.可加入硫酸以提高电解质的导电性
C.充电时,Li+向阳极移动
D.放电时,负极反应式为:2Li0.35NiO2+Li++e-═2Li0.85NiO2
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江哈尔滨三中高三上验收考试三化学卷(解析版) 题型:选择题
能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是
A.加热 B.向水中通CO2 C.加入明矾晶体 D.加入NaHCO3固体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:选择题
己知还取性:SO32->I-。向含有amolKI和amolK2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是
A.当a≥b时,发生的离子反应为SO32-+Cl2+H2O=SO42-+2H++2Cl-
B.当 5a=4b 时,发生的离子反应为 4SO32-+2I-+5Cl2+4H2O=4SO42-+I2+8H++10Cl-
C.当 a≤b≤ 时,反应中转移电子的物质的量n(e-)为 amol≤n(e-)≤3amol
时,反应中转移电子的物质的量n(e-)为 amol≤n(e-)≤3amol
D.当a<b< 时,溶液中SO42-、I-与Cl-的物质的量之比为a:(3a-2b):2b
时,溶液中SO42-、I-与Cl-的物质的量之比为a:(3a-2b):2b
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:选择题
下面有关Na2CO3与NaHCO3的性质比较中错误的是
A.相同浓度溶液的碱性:Na2CO3>NaHCO3
B.同条件下在水中的溶解度:Na2CO3>NaHCO3
C.与同浓度的硫酸反应放出气泡的速率:NaHCO3 <Na2CO3
D.热稳定性:NaHCO3 <Na2CO3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:填空题
常温下,将0.05mol/L盐酸溶液和未知浓度的NaOH溶液以1: 2的体积比混合,所得溶液的pH=12。用上述NaOH溶液滴定pH=3的某一元弱酸溶液20mL,达到终点时消耗NaOH溶液13mL,试求:
(1)NaOH溶液的物质的量浓度为_____________mol/L
(2)此一元弱酸的物质的量浓度为___________mol/L
(3)求此条件下该一元弱酸的电离平衡常数为 ___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁东北育才学校高二上阶段考二化学卷(解析版) 题型:填空题
最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,
总反应为:2CH3CHO+H2O CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH
实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示。
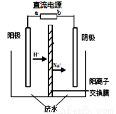
(1)若以甲烷燃料电池为直流电源,则燃料电池中b极应通入 (填化学式)气体。
(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体。电极反应如下:
阳极:① 4OH--4e-=O2↑+2H2O② 。
阴极:① 。②CH3CHO+2e-+2H2O=CH3CH2OH+2OH-
(3)电解过程中,阴极区Na2SO4的物质的量 (填“增大”、“减小”或“不变”)。
(4)电解过程中,某时刻测定了阳极区溶液中各组分的物质的量,其中Na2SO4与CH3COOH的物质的量相同。下列关于阳极区溶液中各微粒浓度关系的说法正确的是 (填字母序号)。
a.c(Na+)不一定是c(SO42-)的2倍
b.c(Na+)=2c(CH3COOH)+2c(CH3COO-)
c.c(Na+)+c(H+)=c(SO 42-)+c(CH3COO-)+c(OH-)
42-)+c(CH3COO-)+c(OH-)
d.c(Na+)>c(CH3COOH)>c(CH3COO-)>c(OH-)
(5)高纯度氧化铝是用于制备隔膜的材料,某研究小组用以下流程制取高纯度氧化铝:
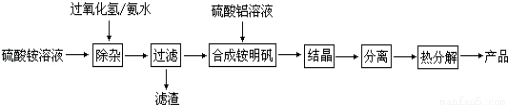
①“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式 。
②配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 。
③“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水)。母液不能蒸干的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com