
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.2.24 L CH4气体中含有的电子数为NA
B.25 ℃时,1.0 L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA
C.0.1NA个氯气分子溶于水形成1 L溶液,所得溶液中c(Cl-)=0.1 mol/L
D.1 mol CH3COONa和少量CH3COOH溶于水形成的中性溶液中,CH3COO-数目为NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014高考化学名师选择题专练 电解质溶液练习卷(解析版) 题型:选择题
向0.1 mol/L的CH3COOH溶液中加水或加入少量CH3COONa晶体时,下列有关叙述不正确的是( )
A.都能使溶液的pH增加
B.都能使溶液中c(H+)·c(CH3COO-)增大
C.都能使溶液中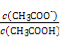 比值增大
比值增大
D.溶液中c(H+)·c(OH-)不变
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学反应中的能量变化练习卷(解析版) 题型:选择题
下列表示物质变化的化学用语中,正确的是( )
A.碱性氢氧燃料电池的负极反应式为O2+2H2O+4e- 4OH-
4OH-
B.用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e- Cl2↑
Cl2↑
C.表示乙炔燃烧热的热化学方程式:C2H2(g)+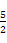 O2(g)
O2(g) 2CO2(g)+H2O(g) ΔH=-1 256 kJ/mol
2CO2(g)+H2O(g) ΔH=-1 256 kJ/mol
D.M与N互为同素异形体,由M N ΔH=+119 kJ/mol可知,N比M稳定
N ΔH=+119 kJ/mol可知,N比M稳定
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 元素周期表元素周期律练习卷(解析版) 题型:选择题
X、Y、Z、T四种原子序数递增的短周期元素,其部分性质或结构如下:
元素编号 | 元素性质或原子结构 |
X | 形成的简单阳离子核外无电子 |
Y | 元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应 |
Z | 元素在周期表的族序数等于周期序数的3倍 |
T | 同周期元素中形成的简单离子半径最小 |
下列说法正确的是( )
A.原子半径大小顺序:T>Z>Y>X
B.常温下,T的单质与Y的最高价氧化物对应水化物的浓溶液反应生成氢气
C.X分别与Y、Z均可形成既含极性键又含非极性键的化合物
D.由X、Y和Z三种元素构成的强电解质,对水电离均起抑制作用
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 元素周期表元素周期律练习卷(解析版) 题型:选择题
下列说法错误的是( )
A.原子最外层电子数为2的元素一定处于周期表ⅡA族
B.主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5
C.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.在0 ℃时,22.4 L氢气中含有2NA个氢原子
B.电解食盐水若产生2 g氢气,则转移的电子数目为NA
C.1 mol乙烷分子中共价键总数为7NA
D.密闭容器中46 g NO2含有的分子数为NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 物质结构与性质练习卷(解析版) 题型:填空题
已知X、Y和Z三种元素的原子序数之和等于48。X是有机物主要组成元素。X的一种1∶1型气态氢化物分子中既有σ键又有π键。Z是金属元素,Z的核电荷数小于28,且次外层有2个未成对电子。
(1)X在该氢化物中以 方式杂化。X和Y形成的化合物的熔点应该 (填“高于”或“低于”)X氢化物的熔点。
(2)Y在周期表中位于 ;Z4+的核外电子排布式为 。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看作一种含氧酸盐)。经X射线分析,M晶体的最小重复单位为正方体(如图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
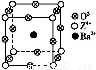
①制备M的化学反应方程式是 (Z用元素符号表示)。
②在M晶体中,Ba2+的氧配位数(Ba2+周围等距且最近的O2-的数目)为 。
③晶体M密度的计算式为ρ= (Z相对原子质量为48)。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 化学实验练习卷(解析版) 题型:实验题
阿司匹林(乙酰水杨酸,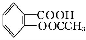 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
乙酸酐+水杨酸
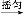
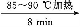
 粗产品
粗产品
 乙酰水杨酸
乙酰水杨酸
(阿司匹林) 测熔点
测熔点
主要试剂和产品的物理常数
名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
水杨酸 | 138 | 158(熔点) | 微溶 |
醋酸酐 | 102 | 139.4(沸点) | 反应 |
乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是 。
(2)①合成阿司匹林时,最合适的加热方法是 。
②加热后冷却,未发现被冷却容器中有晶体析出,此时应采取的措施是 。
③抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是 。
(3)试剂A是 。
另一种改进的提纯方法如下:
粗产品
 乙酰水杨酸
乙酰水杨酸
(4)改进的提纯方法中加热回流的装置如图所示,
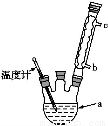
①使用温度计的目的是 。
②此种提纯方法中乙酸乙酯的作用是: ,所得产品的有机杂质要比原方案少,原因是 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题9溶液中的电离平衡练习卷(解析版) 题型:选择题
今有室温下四种溶液,有关叙述不正确的是( )
| ① | ② | ③ | ④ |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH:①>②>④>③
C.①、④两溶液等体积混合,所得溶液中c(Cl-)>c(N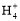 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
D.Va L ④与Vb L ②溶液混合,若混合后溶液pH=4,则Va∶Vb=11∶9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com