
| A、金刚石比石墨稳定 |
| B、1mol石墨比1mol金刚石的总能量低 |
| C、1mol石墨比1mol金刚石的总能量高 |
| D、石墨比金刚石稳定 |


科目:高中化学 来源: 题型:
| A、氧化铝熔点很高,可制造用于熔融烧碱的坩埚 |
| B、炭具有还原性,一定条件下能将二氧化硅还原为硅 |
| C、常温下二氧化硅不与强酸反应,可用石英容器盛放氢氟酸 |
| D、SO2具有漂白性,可用作熏蒸粉丝使其增白 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、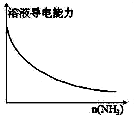 向一定量的CH3COOH溶液中通入NH3至过量 |
B、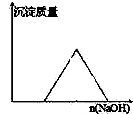 向等物质的量的HCl和AlCl3溶液中滴入NaOH溶液至过量 |
C、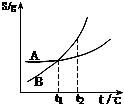 表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液升温至t2℃时,溶质的质量分数B=A |
D、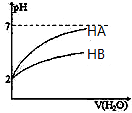 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向硫酸亚铁溶液中通入H2S气体:Fe2++H2S→FeS↓+2H+ |
| B、碳酸钙溶于醋酸:CaCO3+2CH3COOH→Ca2++2CH3COO-+CO2↑+H2O |
| C、少量氢氧化钙溶液与碳酸氢钠溶液混合:OH-+HCO3-→H2O+CO32- |
| D、稀氯化铵溶液和澄清石灰水混合:NH4++OH-→NH3?H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、严禁乱弃废电池,防止重金属污染土壤和水源 |
| B、皮肤沾有苯酚时,立即用氢氧化钠稀溶液擦洗 |
| C、硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料 |
| D、用含有橙色的酸性重铬酸钾的仪器检验酒后驾车,利用了乙醇的挥发性和还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五种阳离子,现用过量的H2SO4、NaOH、NH3?H2O、NaCl四种溶液,按如图所示的步骤分开五种离子.下列判断正确的是( )
某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五种阳离子,现用过量的H2SO4、NaOH、NH3?H2O、NaCl四种溶液,按如图所示的步骤分开五种离子.下列判断正确的是( )| A、沉淀乙是氢氧化铝和氢氧化银的混合物 |
| B、溶液3中含有Al3+ |
| C、溶液4含有三种阳离子,分别是H+、Na+、K+ |
| D、试剂①是NaCl,试剂④是H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.4g | B、8.0g |
| C、8.4g | D、9.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com