
| 实验编号 | 1 | 2 | 3 |
| 实验装置 | 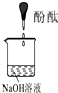 | 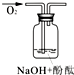 | 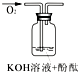 |
| 验证猜想 | ______ | C | ______ |
| 实验现象 | 溶液变红后不退色 | ||
| 实验说明 | 1、2的实验中NaOH溶液是用______(填“氢氧化钠固体”、“氧化钠固体”、“过氧化钠固体”)溶于水配制的. | ||


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源:不详 题型:实验题
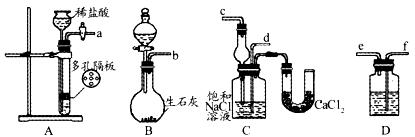
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
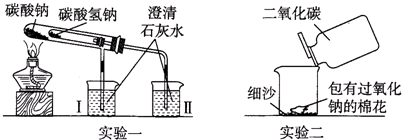
| A.受热时Na2CO3比NaHCO3稳定 |
| B.往Na2CO3和NaHCO3溶液中滴加酚酞都变红,说明Na2CO3和NaHCO3都是碱 |
| C.NaHCO3能转化成Na2CO3,但Na2CO3不能转化成NaHCO3 |
| D.相同物质的量的Na2CO3和NaHCO3分别与足量盐酸反应,消耗盐酸的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
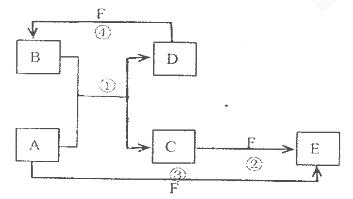
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com