
【题目】根皮素R( )可应用于面膜、护肤膏霜和精华素中。其中一种合成R的路线如下:
)可应用于面膜、护肤膏霜和精华素中。其中一种合成R的路线如下:

已知
①
② +R’’CHO
+R’’CHO +H2O
+H2O
(1)A的化学名称是___________,B→C的反应类型是___________。
(2)D的结构简式是___________,其核磁共振氢谱共有___________组峰。
(3)E→F的化学方程式为___________,G的官能团的名称是___________。
(4)G→H的化学方程式为______________________。
(5)M是F的同分异构体,同时符合下列条件的M的结构有___________种(不考虑立体异构)
①1能与FeCl3溶液发生显色反应 ②能发生银镜反应
(6)设计以丙烯和1,3-丙二醛为起始原料制备![]() 的合成路线___________(无机试剂任选)。
的合成路线___________(无机试剂任选)。
【答案】苯酚 取代反应 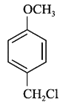 4
4  (酚)羟基、醛基
(酚)羟基、醛基 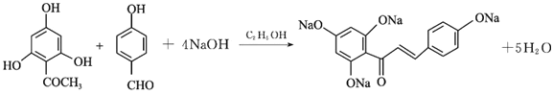 13
13 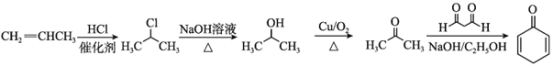
【解析】
有机物A(C6H6O)和CH3Cl在无水氯化铝做催化剂的条件下发生取代反应生成B(C7H8O),B和氯气在光照的条件下发生取代反应生成C,由C的结构简式可推出A为苯酚,B为对甲基苯酚;C和CH3I发生取代反应生成D,由已知①可知D的结构简式为![]() ;D和氢氧化钠溶液加热发生水解反应生成E,E在铜作催化剂的条件下发生催化氧化生成F,由F的结构可推知E的结构简式为
;D和氢氧化钠溶液加热发生水解反应生成E,E在铜作催化剂的条件下发生催化氧化生成F,由F的结构可推知E的结构简式为![]() ;F和HI加热生成G,结合已知①,G的结构简式为
;F和HI加热生成G,结合已知①,G的结构简式为![]() ;
;
根据已知②G和I生成H,H经酸化得到J,J的结构简式为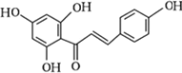 ,J经反应得到R,以此分析解答。
,J经反应得到R,以此分析解答。
(1)根据以上分析,A的化学名称是苯酚;B和氯气在光照的条件下发生取代反应生成C,所以B→C的反应类型是取代反应,
故答案为:苯酚;取代反应;
(2)D的结构简式是![]() ,分子中有4种类型的氢原子,其核磁共振氢谱共有4组峰,
,分子中有4种类型的氢原子,其核磁共振氢谱共有4组峰,
故答案为:![]() ;4;
;4;
(3) E的结构简式为![]() ,E在铜作催化剂的条件下发生催化氧化生成F,所以E→F的化学方程式为
,E在铜作催化剂的条件下发生催化氧化生成F,所以E→F的化学方程式为 ;G的结构简式为
;G的结构简式为![]() ,含有的官能团的名称是(酚)羟基、醛基,
,含有的官能团的名称是(酚)羟基、醛基,
故答案为: ;(酚)羟基、醛基;
;(酚)羟基、醛基;
(4) 根据已知②G和I生成H,G→H的化学方程式为 ,
,
故答案为: ;
;
(5)F的结构简式为![]() ,M是F的同分异构体,符合条件①能与FeCl3溶液发生显色反应说明含有酚羟基,②能发生银镜反应说明含有醛基,可能的结构有:
,M是F的同分异构体,符合条件①能与FeCl3溶液发生显色反应说明含有酚羟基,②能发生银镜反应说明含有醛基,可能的结构有:
苯环上有一个-OH、一个-CHO和一个-CH3共有10种;
苯环上有一个-OH和一个HCOOCH2-,处于邻、间、对共3种;所以共有13种,
故答案为:13;
(6)根据已知②,结合题给原料1,3-丙二醛和丙烯,若要制备![]() ,需要由丙烯制得丙酮,丙酮和1,3-丙二醛发生已知②的反应得到
,需要由丙烯制得丙酮,丙酮和1,3-丙二醛发生已知②的反应得到![]() 。所以具体的合成路线设计为:
。所以具体的合成路线设计为: ,
,
故答案为: 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】硫酸锌可用于制造锌钡白、印染媒染剂等。用锌白矿(主要成分为ZnO,还含有FeO、CuO、SiO2等杂质)制备ZnSO4·7H2O的流程如下。
已知:Ksp[Fe(OH)3]=4.0×1038,Ksp[Cu(OH)2]=2.2×1020

(1)“滤渣1”的主要成分是_______(填化学式)。“酸浸”过程中,为了提高锌元素浸出速率,可采取的措施有:①适当提高酸的浓度,②_______(填一种)。
(2)“氧化”过程中,发生氧化还原反应的离子方程式是_______。
(3)“沉淀”过程中,加入ZnO产生Fe(OH)3沉淀的原因是_______。
(4)加入适量ZnO固体,若只析出Fe(OH)3沉淀而未析出Cu(OH)2沉淀,且测得沉淀后的溶液中c(Fe3+)=4.0×1014mol/L,此时溶液中c(Cu2+)的取值范围是_______mol/L。
(5)加入适量锌粉的作用是_______。
(6)由滤液得到ZnSO47H2O的操作依次为_______、_______、过滤、洗涤、干燥。实验室中过滤操作需要使用的玻璃仪器有烧杯、_______、_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组用如图装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则A极的电极反应式为____________________B极的Fe发生__________ 腐蚀(填“析氢”或“吸氧”)
(2)若开始时开关K与b连接,下列说法正确的是________(填序号)
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子且此时装置内总反应的离子方程式为_________
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为______________,此时通过阴离子交换膜的离子数________(填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口________(填“A”“B”“C”或“D”)导出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A. 1.9gH3O+中含质子总数为NA
B. 体积均为22.4L(标准状况)的乙烯和乙酸含氢原子数均为4NA
C. 1L0.1mol·L-1NH4A1(SO4)2溶液中阳离子总数小于0.2NA
D. 当反应MgO+C+Cl2![]() MgCl2+CO中断裂2 mol Cl-Cl键时,转移电子总数为4NA
MgCl2+CO中断裂2 mol Cl-Cl键时,转移电子总数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种利用化肥中废催化剂(含CoO、Co、Al2O3及少量FeO)制取明矾和CoSO4粗产品的工艺流程如下:

已知:(i)相关金属离子形成氢氧化物沉淀的pH范围如下表所示:

(ⅱ)Al(OH)3在碱性条件下开始溶解时的pH为7.8,完全溶解时的pH为11。
回答下列问题:
(1)写出H2O2的电子式:___________。
(2)下列措施一定能提高步骤I中A13+和Co2+的浸取率的是___________(填标号)
a.将废催化剂粉磨为细颗粒
b.步骤I中的硫酸采用98%的浓硫酸
c.适当提高浸取时的温度
(3)步骤Ⅱ中,写出“氧化”过程中Fe2+被氧化的离子方程式:___________,若“氧化”后再“调节pH=3”,造成的后果是___________。
(4)步骤Ⅲ中加K2CO3应控制pH的范围为___________。
(5)测定CoSO4粗产品中钴的质量分数的步骤如下:准确称取ag产品,先经预处理,然后加入过量的冰乙酸,在加热煮沸下,缓慢滴加KNO2溶液直至过量,生成不溶于乙酸的K3[Co(NO2)6],再经过滤、洗涤及干燥,称量沉淀的质量为bg。
①KNO2溶液氧化并沉淀Co2+的离子方程式为___________(已知KNO2被还原为NO)。
②粗产品中钴元素的质量分数为___________(Mr{K3[Co(NO2)6]}=452,列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了将混有K2SO4、MgSO4、CaCl2的KCl固体提纯,并制得纯净的KCl晶体,某同学设计如下实验方案,请回答下列问题:

(1)操作⑤⑥的名称依次为___、___。
(2)操作②、③加入溶液后,发生反应的离子方程式分别为___、___。
(3)该同学设计的实验方案___(填“严密”或“不严密”),理由是___,该步骤所加试剂应该是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备乙酸丁酯的装置如图所示,下列分析错误的是

A. 加入过量乙酸可以提高丁醇的转化率
B. 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
C. 导气管a起到冷凝回流的作用
D. 制乙酸丁酯的反应温度超过100℃不能用水浴加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有解热镇痛及抗生素作用的药物“芬必得”主要成分的结构简式如图,它属于( )

①芳香族化合物 ②脂肪族化合物 ③有机羧酸 ④有机高分子化合物 ⑤芳香烃
A. ③⑤ B. ②③ C. ①③ D. ①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com