
某烃结构简式如下: -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )
A.所有原子可能在同一平面上
B.所有原子可能在同一条直线上
C.所有碳原子可能在同一平面上
D.所有氢原子可能在同一平面上
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源:2015届辽宁省高三上学期期初检测化学试卷(解析版) 题型:选择题
下列各组离子,一定能在指定环境中大量共存的是
A.在含有大量I-离子的溶液中:Cl?、Fe3+、Al3+、Cu2+
B.滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl-、NO3-能够大量共存
C.在由水电离出的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、Cl?、Br?
D.在加入Al能放出大量H2的溶液中:NH4+、SO42? 、C1?、HCO3?
查看答案和解析>>
科目:高中化学 来源:2015届贵州省贵阳市高三8月月考理综化学试卷(解析版) 题型:选择题
向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示。下列判断正确的是
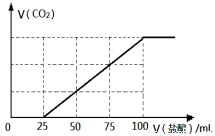
A.原NaOH溶液的浓度为0.2 mol/L
B.通入CO2的体积为448 mL
C.所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3) = 1: 3
D.所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3) = 1: 1
查看答案和解析>>
科目:高中化学 来源:2015届福建省福州八市高二下学期期中考试化学试卷(解析版) 题型:选择题
某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是( )
A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和
查看答案和解析>>
科目:高中化学 来源:2015届福建省福州八市高二下学期期中考试化学试卷(解析版) 题型:选择题
下列物质中可以使蛋白质变性的是( )
①福尔马林;②酒精;③高锰酸钾溶液;④硫酸铵溶液;⑤硫酸铜;⑥双氧水;⑦硝酸
A.除④、⑦外 B.除③、⑥外 C.①②⑤ D.除④外
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三上学期第一次检测考试化学试卷(解析版) 题型:填空题
(18分)I.某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。
已知该反应中H2O2只发生如下过程:H2O2→O2。
(1) 该反应中的还原剂是________。
(2) 该反应中,发生还原反应的过程是________→________。
(3) 写出该反应的化学方程式,并标出电子转移的方向和数目:
_____________________ __ 。
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为________。
II.高锰酸钾在不同的条件下发生的反应如下:
MnO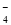 +5e-+8H+===Mn2++4H2O ①
+5e-+8H+===Mn2++4H2O ①
MnO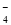 +3e-+2H2O===MnO2↓+4OH- ②
+3e-+2H2O===MnO2↓+4OH- ②
MnO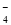 +e-===MnO
+e-===MnO (溶液绿色) ③
(溶液绿色) ③
(1) 从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的________影响。
(2) 将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为
__________→___________。
(3) 将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是________
a. 氧化性:PbO2>KMnO4
b. 还原性:PbO2>KMnO4
c. 该反应可以用盐酸酸化
(4) 将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3∶2, 完成下列化学方程式(横线上填系数,括号内填物质):
① ________KMnO4+________K2S+______( )===________K2MnO4+________K2SO4+________S↓+______( )。
② 若生成6.4g单质硫,反应过程中转移电子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三上学期第一次检测考试化学试卷(解析版) 题型:选择题
下列有关Fe2(SO4)3溶液的叙述正确的是( )
A.该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存
B.和KI溶液反应的离子方程式:
Fe3++2I-===Fe2++I2
C.和Ba(OH)2溶液反应的离子方程式:Fe3++SO +Ba2++3OH-===Fe(OH)3↓+BaSO4↓
+Ba2++3OH-===Fe(OH)3↓+BaSO4↓
D.1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高三第一次模拟考试化学试卷(解析版)) 题型:填空题
(每空2分,作图3分,共13分)某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是Al3+和________,阴离子是________。
(2)试通过计算确定:n(Al3+)=________;该结晶水合物的化学式________ 。
(3)假设过程中向该溶液中加入的Ba(OH)2溶液的物质的量浓度为2.0mol/L。
①加入 mLBa(OH)2溶液时,所得沉淀的总物质的量最大。
②请在下图中画出生成沉淀的物质的量与加入Ba(OH)2溶液体积的关系示意图。

查看答案和解析>>
科目:高中化学 来源:2015届湖南省高三第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.H、D、T属于同位素,H2、D2、T2属于同素异形体
B.氯水、氨水、王水是混合物,水银、水玻璃是纯净物
C.冰醋酸、纯碱、小苏打分别属于酸、碱、盐
D.水能、风能、生物质能是可再生能源,煤、石油、天然气是不可再生能源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com