
 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | c(H+)=1×10-13mol/L的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| C. | 加入铝粉产生氢气的溶液:Na+、K+、SO42-、Cl- | |
| D. | $\frac{c{(H}^{+})}{c({OH}^{-})}$=1×1014的溶液:Ca2+、Na+、ClO-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=30mol•L-1•min-1 | B. | v(B)=0.3mol•L-1•s-1 | ||
| C. | v(C)=48mol•L-1•min-1 | D. | v(D)=1mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎把浓硫酸粘在手上,立即用大量的水冲洗,涂上3%-5%的碳酸氢钠溶液 | |
| B. | 如果汽油、煤油等可燃物着火,应立即用沙土扑灭 | |
| C. | 不慎将浓碱沾到皮肤上,立即用大量的水冲洗,然后涂上硼酸溶液 | |
| D. | 酒精灯不慎碰翻着火,应立即用湿布盖灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a=b且pH(NaX)>pH(NaY),则酸性HX<HY | |
| B. | 若a=b且c(X -)=c(Y -)+c(HY),则酸性HX>HY | |
| C. | 若a>b且c(X -)=c(Y -),则酸性HX<HY | |
| D. | 若a=0.1mol/L且两溶液等体积混合,则c(X -)+c(HX)=0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol CH4含有的电子数为NA | |
| B. | 标准状况下,22.4L己烷中共价键数为19NA | |
| C. | 6.4g CaC2固体中所含阴离子数为0.2NA | |
| D. | 1L 1mol/L的NaHCO3溶液中含有NA个HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1MgCl2溶液 | B. | 0.1mol•L-1NH4Cl溶液 | ||
| C. | 0.1mol•L-1KCl溶液 | D. | 0.1mol•L-1 AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
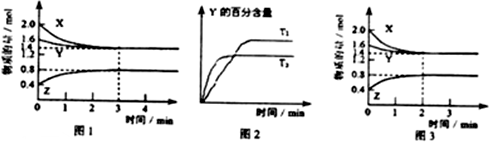
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com