B
分析:A、铝离子在溶液中发生水解,铝离子的浓度小于2mol/L.
B、铜元素在Cu
2S和CuO中的质量分数相同,混合物中铜元素的质量分数为
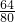
.据此计算铜元素质量,根据n=

计算铜物质的量,根据N=nN
A计算铜原子数.
C、根据n=

计算重水的物质的量,每个分子含有10个电子,根据N=nN
A计算电子数.
D、在标准状况下,22.4LNO与11.2LO
2混合恰好反应生成二氧化氮,NO
2存在平衡:2NO
2?N
2O
4.据此计算判断.
解答:A、1mol/LAl
2(SO
4)
3溶液中SO
42-的浓度为3mol/L,Al
3+离子在溶液中发生水解,Al
3+的浓度小于2mol/L,所以溶液中Al
3+和SO
42-离子的总浓度小于5mol/L,故200ml该溶液中Al
3+和SO
42-总的物质的量小于0.2L×5mol/L=1mol,所以Al
3+和SO
42-总数小于N
A,故A错误;
B、铜元素在Cu
2S和CuO中的质量分数相同,混合物中铜元素的质量分数为
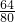
,所以8gCu
2S和CuO的混合物中铜元素的质量为
8g×
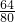
=6.4g,所以含有的铜原子数目为

×N
Amol
-1=0.1N
A,故B正确;
C、18.0g重水(D
2O)的物质的量为

=0.9mol,每个分子含有10个电子,18.0g重水(D
2O)所含的电子数为
0.9mol×10×N
Amol
-1=9N
A,故C错误;
D、NO与O
2在标况下反应生成NO
2,由反应2NO+O
2=2NO
2可知,22.4LNO与11.2LO
2恰好反应生成22.4LNO
2,NO
2存在平衡:
2NO
2?N
2O
4,所以混合气体的体积小于22.4L,标准状况下,混合气体的物质的量小于1mol,气体的总的分子数小于N
A,故D错误.
故选:B.
点评:考查常用化学计量数的有关计算,难度中等,B选项关键在于根据相对分子质量分析铜元素的质量分数,选项D为易错点,容易忽略平衡2NO
2?N
2O
4.

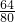 .据此计算铜元素质量,根据n=
.据此计算铜元素质量,根据n= 计算铜物质的量,根据N=nNA计算铜原子数.
计算铜物质的量,根据N=nNA计算铜原子数. 计算重水的物质的量,每个分子含有10个电子,根据N=nNA计算电子数.
计算重水的物质的量,每个分子含有10个电子,根据N=nNA计算电子数.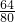 ,所以8gCu2S和CuO的混合物中铜元素的质量为
,所以8gCu2S和CuO的混合物中铜元素的质量为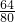 =6.4g,所以含有的铜原子数目为
=6.4g,所以含有的铜原子数目为 ×NAmol-1=0.1NA,故B正确;
×NAmol-1=0.1NA,故B正确; =0.9mol,每个分子含有10个电子,18.0g重水(D2O)所含的电子数为
=0.9mol,每个分子含有10个电子,18.0g重水(D2O)所含的电子数为

 阅读快车系列答案
阅读快车系列答案