
A、 |
| B、CH3COOCH3 |
| C、2-氯丙烷 |
D、 |
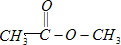 不对称,有2种H原子,则核磁共振氢谱中出现2组峰,氢原子数之比为1:1,
不对称,有2种H原子,则核磁共振氢谱中出现2组峰,氢原子数之比为1:1,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、弱电解质的电离平衡常数受温度影响,与溶液浓度无关 |
| B、电离平衡常数表达了弱电解质的电离能力 |
| C、多元弱酸水溶液中的H+主要是第一步电离产生的 |
| D、由于Ka[HF]>Ka[CH3COOH]>Ka[HCN],所以酸性顺序HF<CH3COOH<HCN |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C6H5CH2OH 酚类-OH |
| B、CH3CH2COOH 羧酸-COOH |
| C、HCOOCH3 醛类-CHO |
| D、H3CCH2CH3 烃类-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、室温下,NaR溶液的pH大于7 |
| B、加热NaR溶液时,溶液的pH变小 |
| C、将锌粒分别投入到1 mol?L-1的盐酸和HR中,HR产生氢气的速率慢 |
| D、室温下,0.1 mol?L-1HR的pH>1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 )是食品添加剂的增香原料,其合成路线如图:
)是食品添加剂的增香原料,其合成路线如图: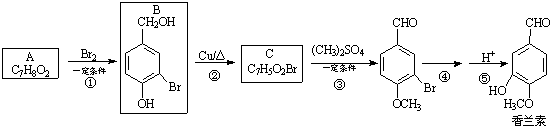

| (CH3)2SO4 |
| 一定条件 |
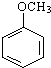
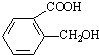 ,在一定条件下可以合成聚酯高分子,写出该聚酯高分子的结构简式
,在一定条件下可以合成聚酯高分子,写出该聚酯高分子的结构简式查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com