
��1�������������յĻ�ѧ֪ʶ���������жϣ�������ʹ�õ�Һ̬���ۼ�֮һ�ض����ȣ�����������ܵĴ�����ʽ��______________��________________�������ӣ�������һ�־���_______________�����ʣ���Һ̬���ۼ���֮��ϣ����ܷ���������Ӧ����������������˵�������ֽ��ۼ������ƣ����ý��ۼ�����Ʒ���ƣ���_________________��_________________��
��2��������г��ϵĽ��ۼ����з�����飬������������ͳ�ƺ������ѧ��֪ʶ�Ը���Ʒ�ƵĽ��ۼ����з�������Ϊ������ָ��ʹ�ò�ͬ���͵Ľ��ۼ�ʱӦע������⡣
______________________________________________________________________
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ���ܵ���� | AgI | AgOH | Ag2S | PbI2 | Pb��OH��2 | PbS |
| Ksp | 8.3��10-17 | 5.6��10-8 | 6.3��10-50 | 7.1��10-9 | 1.2��10-15 | 3.4��10-28 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�038
��1�������������յĻ�ѧ֪ʶ���������жϣ�������ʹ�õ�Һ̬���ۼ�֮һ�ض����ȣ�����������ܵĴ�����ʽ��______________��________________�������ӣ�������һ�־���_______________�����ʣ���Һ̬���ۼ���֮��ϣ����ܷ���������Ӧ����������������˵�������ֽ��ۼ������ƣ����ý��ۼ�����Ʒ���ƣ���_________________��_________________��
��2��������г��ϵĽ��ۼ����з�����飬������������ͳ�ƺ������ѧ��֪ʶ�Ը���Ʒ�ƵĽ��ۼ����з�������Ϊ������ָ��ʹ�ò�ͬ���͵Ľ��ۼ�ʱӦע������⡣
______________________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
±�ص��ʵ����ʻ��ã�±�صĻ�����Ӧ�ù㷺���о�±�ص��ʼ��仯���������Ҫ���塣
��1�������������ر�����ת���˲�Ҫ����ͬƷ�ƽ��ۼ����ʹ�õľ��档�ݱ�������ȫ�����ط����˶����Ͻ��ۼ����������ж����¼���������Ļ�ѧ֪ʶ���������жϣ�
������ʹ�õ�Һ̬���ۼ�֮һ�ض����ȣ�����ܵĴ�����ʽ�������� �������� ������һ�־������������� �����ʣ���Һ̬���ۼ���֮��ϣ����ܷ������·�Ӧ������������������������������������
��
(2)�������ε������Խ�ǿ�����ڼ��Ի����н�����������������������佫Fe3+����Ϊ����ɱ��������FeO42-��д���÷�Ӧ�����ӷ���ʽ ��
(3)���ٵƾ��бȰ׳���������һ������ܵ��ص㡣һ���¶��£������ڷ�����������ʹ�ù����г����ڹܱ��ϵ��ٿ��Է�����Ӧ��
W(s)+I2(g)![]() WI2(g)��Ϊģ��������Ӧ��ȷ��ȡ0.508g�⡢0.736g����������50.0mL���ܱ������У� ����ʹ�䷴Ӧ��
WI2(g)��Ϊģ��������Ӧ��ȷ��ȡ0.508g�⡢0.736g����������50.0mL���ܱ������У� ����ʹ�䷴Ӧ��
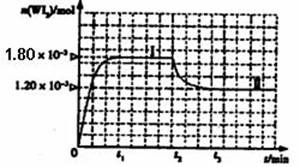
��ͼ��WI2(g)�����ʵ�����ʱ��仯��ϵͼ����������I(0~t2ʱ���)�ķ�Ӧ�¶�ΪT1������II(��t2��ʼ)�ķ�Ӧ�¶�ΪT2����T2>T1��ks*5*u
|
|
|
|

�ٸ÷�Ӧ�ġ�H 0(�>�� ��=����<��)
�ڴӷ�Ӧ��ʼ��t1ʱ���ڵ�ƽ����Ӧ����v(I2)= ��
������˵���в���ȷ���� (�����)��
A���÷�Ӧ��ƽ�ⳣ������ʽ��![]()
B����˿�����¶�Խ�ߣ���˿��������WI2Խ�ױ�ΪW�����³�������˿��
C�����ø÷�Ӧԭ�������ᴿ��
(4)25��ʱ����5mL����KCl��KIŨ�Ⱦ�Ϊ0.1mol/L�Ļ��Һ�У��μ�6mL0.1mol/L��AgNO3��Һ����Һ������Ũ���ɴ�С��˳���� ��
[������H+��OH-��25��ʱKSP(AgCl)=1.8��10-10��KSP(AgI)=8.3��10-17]��
(5)Mg�������ᴿTi���Լ�����֪��
��Mg(s)+Cl2(g)=MgCl2(s) ��H= ��641kJ/mol ��Ti(s)+2Cl2(g)=TiCl4(l) ��H= ��770kJ/mol
��д��Mg��Һ̬TiCl4��Ӧ�ᴿ�ѵ��Ȼ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
±�ص��ʵ����ʻ��ã�±�صĻ�����Ӧ�ù㷺���о�±�ص��ʼ��仯���������Ҫ���塣
��1�������������ر�����ת���˲�Ҫ����ͬƷ�ƽ��ۼ����ʹ�õľ��档�ݱ�������ȫ�����ط����˶����Ͻ��ۼ����������ж����¼���������Ļ�ѧ֪ʶ���������жϣ�
������ʹ�õ�Һ̬���ۼ�֮һ�ض����ȣ�����ܵĴ�����ʽ�������� �������� ������һ�־������������� �����ʣ���Һ̬���ۼ���֮��ϣ����ܷ������·�Ӧ������������������������������������
��
(2)�������ε������Խ�ǿ�����ڼ��Ի����н�����������������������佫Fe3+����Ϊ����ɱ��������FeO42-��д���÷�Ӧ�����ӷ���ʽ ��
(3)���ٵƾ��бȰ׳���������һ������ܵ��ص㡣һ���¶��£������ڷ�����������ʹ�ù����г����ڹܱ��ϵ��ٿ��Է�����Ӧ��
W(s)+I2(g)![]() WI2(g)��Ϊģ��������Ӧ��ȷ��ȡ0.508g�⡢0.736g����������50.0mL���ܱ������У� ����ʹ�䷴Ӧ��
WI2(g)��Ϊģ��������Ӧ��ȷ��ȡ0.508g�⡢0.736g����������50.0mL���ܱ������У� ����ʹ�䷴Ӧ��
��ͼ��WI2(g)�����ʵ�����ʱ��仯��ϵͼ����������I(0~t2ʱ���)�ķ�Ӧ�¶�ΪT1������II(��t2��ʼ)�ķ�Ӧ�¶�ΪT2����T2>T1��
|
|
|
|
�ٸ÷�Ӧ�ġ�H 0(�>�� ��=����<��)
�ڴӷ�Ӧ��ʼ��t1ʱ���ڵ�ƽ����Ӧ����v(I2)= ��
������˵���в���ȷ���� (�����)��
A���÷�Ӧ��ƽ�ⳣ������ʽ��![]()
B����˿�����¶�Խ�ߣ���˿��������WI2Խ�ױ�ΪW�����³�������˿��
C�����ø÷�Ӧԭ�������ᴿ��
(4)25��ʱ����5mL����KCl��KIŨ�Ⱦ�Ϊ0.1mol/L�Ļ��Һ�У��μ�6mL0.1mol/L��AgNO3��Һ����Һ������Ũ���ɴ�С��˳���� ��
[������H+��OH-��25��ʱKSP(AgCl)=1.8��10-10��KSP(AgI)=8.3��10-17]��
(5)Mg�������ᴿTi���Լ�����֪��
��Mg(s)+Cl2(g)=MgCl2(s) ��H= ��641kJ/mol ��Ti(s)+2Cl2(g)=TiCl4(l) ��H= ��770kJ/mol
��д��Mg��Һ̬TiCl4��Ӧ�ᴿ�ѵ��Ȼ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com