
下列表示对应化学反应的离子方程式.其中正确的是
A.向NaAlO2溶液中通入过量的CO2:2AlO2﹣+CO2+3H2O═2Al(OH)3↓+CO32﹣
B.NH4HCO3溶液中加入过量氢氧化钠溶液:NH4++OH﹣═ NH3.H2O
C.AlCl3溶液中滴加过量氨水:Al3+ + 3NH3.H2O ═ 3NH4++ Al(OH)3↓
D.磁性氧化铁(Fe3O4)溶于稀硝酸3Fe2++4H++NO3﹣═3Fe3++NO↑+2H2O
科目:高中化学 来源:2015-2016学年吉林省高一入学摸底化学试卷(解析版) 题型:实验题
(Ⅰ)下列操作会导致实验结果偏高的是 。
A.配制一定物质的量浓度的硫酸溶液时,定容摇匀后,发现液面低于刻度线
B.在配制一定物质的量浓度溶液时,用10 mL的量筒量取5.0 mL液体溶质时俯视读数
C.用天平称量20.5 g某物质,砝码和药品的位置放反,所得药品的质量
D.配制一定物质的量浓度的溶液时,定容时俯视读数,所得溶液的浓度
(Ⅱ)现有下列仪器或用品:
a铁架台(含铁圈、铁夹);
b锥形瓶;
c滴定管;
d烧杯(若干);
e玻璃棒;
f胶头滴管;
g托盘天平(含砝码);
h滤纸;
i量筒;
j漏斗;
k温度计
现有下列试剂:
A.NaOH固体 B.碳酸钠溶液
C.氯化镁溶液 D.蒸馏水
试填空:
(1)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是 。
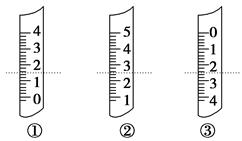
A.①是量筒,读数为1.5 mL
B.②是量筒,读数为2.50 mL
C.③是滴定管,读数为2.50 mL
D.①是温度计,读数是1.50 ℃
(2)配制100 mL 0.1 mol·L-1的氢氧化钠溶液时,还缺少的仪器有 。
(3)除去Mg(OH)2中混有的少量Ca(OH)2,可以用到的试剂是(选填序号),操作方法是 、 、洗涤。完成上述操作,上述仪器或用品用到的有(从上述仪器或用品中选择,填上相应序号)。
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三9月月考化学试卷(解析版) 题型:选择题
在一密闭容器中有CO、H2、O2共16.5g和足量的Na2O2,用电火花引燃,使其完全反应,Na2O2增重7.5g,则原混合气体中O2的质量分数是
A.54.5% B.40% C.36% D.33.3%
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期入学考试化学试卷(解析版) 题型:填空题
(16分)FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:(16分)
(1)FeCl3 净水的原理是 。FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3 。
①若酸性FeCl2 废液中各离子浓度如下:则该溶液的pH约为 。
c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,
②NaClO3 能在酸性条件下氧化FeCl2 ,写出离子方程式:
(3)FeCl3 在溶液中分三步水【解析】
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为: xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。
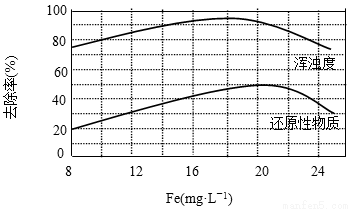
由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省遵义市高三上学期第一次月考化学试卷(解析版) 题型:选择题
已知反应X+Y=M+N为放热反应,对这个反应的下列说法中正确的是
A.X的能量一定高于M的,Y的能量一定高于N的
B.因为该反应为放热反应,故一定不需要加热就能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.因为该反应为放热反应,一定可以设计为原电池将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上化学试卷(解析版) 题型:选择题
电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一项重大贡献。下列有关电池的叙述正确的是
A.锌锰干电池工作一段时间后碳棒变细
B.氢氧燃料电池可将热能直接转变为电能
C.氢氧燃料电池工作时氢气在负极被氧化
D.太阳能电池的主要材料是高纯度的二氧化硅
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁葫芦岛一中高二上期初考试化学试卷 (解析版) 题型:选择题
下列各组中化合物的性质比较,不正确的是
A.酸性:HClO4>HBrO4>HIO4 B.稳定性:PH3>H2S> HCl
C.碱性:NaOH>Mg(OH)2>Al(OH)3 D.非金属性F>O>S
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三9月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.用活性炭去除冰箱中的异味是发生了化学反应
B.用热碱水清除炊具上残留的油污,是因为Na2CO3可直接和油污反应
C.用浸泡过高锰酸钾溶液的硅藻土保存水果
D.漂白粉在空气中久置变质是因为漂白粉中的CaCl2 与空气中的CO2反应生成CaCO3
查看答案和解析>>
科目:高中化学 来源:2016届广西河池市高三上学期第一次月考理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.第ⅠA族元素是周期表中金属性最强的金属元素
B.两个非金属原子间不可能形成离子键
C.HF、HCl、HBr和HI的热稳定性和还原性依次减弱
D.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com