
| A. | a1>a2,c1>c2 | B. | a1<a2,c1<c2 | C. | a1>a2,c1<c2 | D. | a1<a2,c1>c2 |
科目:高中化学 来源: 题型:选择题
| A. | 稀醋酸中加入少量醋酸钠固体能增大醋酸的电离程度 | |
| B. | 室温下,氨水加水稀释后,溶液中c(NH4+)•c(OH-)变大 | |
| C. | NaHCO3溶液中溶质的电离方程式为NaHCO3=Na++H++CO32- | |
| D. | 强电解质溶液导电能力不一定强于弱电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 向一容积为5L的恒容密闭容器内,充入0.2mol CO和0.4mol H2O,在一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H>0.反应中CO2的浓度(c) 随时间(t)的变化关系如图所示.
向一容积为5L的恒容密闭容器内,充入0.2mol CO和0.4mol H2O,在一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H>0.反应中CO2的浓度(c) 随时间(t)的变化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
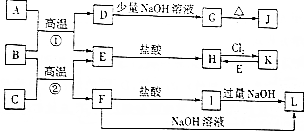
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释Na2CO3溶液时,$\frac{c(HC{{O}_{3}}^{-}•c(O{H}^{-}))}{c(C{{O}_{3}}^{2-})}$增大 | |
| B. | 常温下,反应4Fe(OH)2(s)+2H2O(I)+O2(g)═4Fe(OH)3(s)的△H<0,△S<0 | |
| C. | 用0.1mol•L-1CH3COOH溶液滴定0.1mol•L-1 NaOH至中性时:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| D. | 向纯水中加入盐酸或氢氧化钠都能使水的电离平衡逆向移动,水的离子积减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl- | B. | Al3+ | C. | Fe3+ | D. | NH${\;}_{4}^{+}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将4gNaOH溶液溶入1L水中 | |
| B. | 常温下,将2.24LHCl气体溶于水配成1L溶液 | |
| C. | 含有4.9gH2SO4的溶液500mL | |
| D. | 将6.2gNa2O溶于水配成1L溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | N≡N | H-N |
| 键能 | 436kJ/mol | 946kJ/mol | x |
| A. | 391kJ/mol | B. | 431kJ/mol | C. | 349kJ/mol | D. | 469kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com