
| A. | A原子最外层电子数比B原子最外层电子数少 | |
| B. | A的最高价氧化物对应水化物的碱性强于B的最高价氧化物对应水化物的碱性 | |
| C. | 1molA与足量酸反应生成的H2比1molB与足量酸反应生成的H2多 | |
| D. | 常温时,A、B均能导电,且导电性良好 |
分析 比较金属的活泼性可根据金属之间的置换反应及金属与酸反应置换氢气的难易程度判断,金属与水反应的难易程度,最高价氧化物的水化物碱性,原电池的正负极判断等方面判断,不能从电子层的多少、最外层电子数的多少以及生成氢气的多少的角度判断.
解答 解:A、如金属不位于同一主族,则不能根据电子层数的多少来判断金属的活泼性强弱,故A错误;
B、最高价氧化物的水化物碱性越强,其元素的非金属性越强,A的最高价氧化物对应水化物的碱性强于B的最高价氧化物对应水化物的碱性,可以说明金属A的活动性比金属B的活动性强,故B正确;
C、产生氢气的多少取决于金属失去电子数的多少,金属的活泼性与得失电子难易有关,与得失电子数目无关,故C错误;
D、金属的导电性属于物理性质,不能根据导电性来判断金属性的强弱,故D错误;
故选B.
点评 本题考查了金属活泼性的判断方法,要注意的是:金属的金属性强弱与得失电子的难易有关,与得失电子的多少无关,题目难度不大.


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:选择题
| A. |  除去CO2中的HCl | B. |  蒸发氯化钠溶液 | ||
| C. |  稀释浓硫酸 | D. |  过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,⑦的电子式是
,⑦的电子式是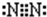 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若XY4分子中X原子处于正四面体的中心,则XY4分子为非极性分子 | |
| B. | C2H5OH与C2H5Br相比,前者的相对分子质量远小于后者,而沸点却远高于后者,其原因是前者的分子间存在氢键 | |
| C. | CO2与SiO2晶体熔化时,所克服的微粒间相互作用相同 | |
| D. | 短周期元素离子aXm+和bYn-具有相同的电子层结构,则a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
| S | 112.8 | 444.6 | 略 |
| S2Cl2 | -77 | 137 | 遇水生成HCl、SO2、S 3000C以上完全分解 |

| 实验步骤 | 实验现象和结论 |
| 1.取少量溶液于试管中,滴入几滴KMnO4溶液 | KMnO4溶液颜色由紫色变绿色,说明溶液中大量存在SO32- |
| 2.另取少量溶液于试管中,加入2-3滴酚酞溶液 | 溶液颜色由无色变红,说明溶液中大量存在OH- |
| 3.另取少量溶液于试管中,加入足量1mol•L-1HNO3,再加入少量AgNO3溶液 | 仍有白色沉淀产生,说明溶液中大量存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤⑥⑦ | B. | ②③④⑤ | C. | ①②④⑤⑥⑦ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1NH4Cl溶液的KW大于0.01mol?L-1NH4Cl溶液的KW | |
| B. | 当镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大 | |
| D. | 水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com