
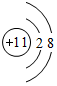 .
.
分析 I.X、Y、Z均为短周期元素,X的单质为密度最小的气体,则X为氢元素,Z与X原子最外层电子数相同,则Z处于IA族,Y的最高化合价与最低负价的代数和为2,则Y处于VA族,结合X、Y、Z的原子序数依次增大,可推知Y为N元素、Z为Na元素.
(1)钠离子核外有10个电子,有2个电子层,各层电子数为2、8;
(2)X和Y组成的化合物Q中,既含有极性共价键又含有非极性共价键,则Q为N2H4,Q在空气中燃烧产物没有任何污染,则反应生成氮气与水.Q还可将酸性工业废水中的Cr2O72-还原为Cr3+,氧化产物为常见气体,则氧化产物为氮气,结合电子转移守恒、电荷守恒与原子守恒配平;
Ⅱ.(3)双氧水中两个氢原子分别与两个氧原子通过共用一对电子结合,两个氧原子之间通过共用1对电子结合;
(4)双氧水可以将废水中的氰化物转化为无毒物同时生成NH3,其中碳元素的化合价升高,结合原子守恒和电荷守恒可知无毒的物质是碳酸氢钠,配平书写离子方程式;
(5)铁离子会加速H2O2分解,三价铁离子和碳酸根的水解双促进.
解答 解:I.X、Y、Z均为短周期元素,X的单质为密度最小的气体,则X为氢元素,Z与X原子最外层电子数相同,则Z处于IA族,Y的最高化合价与最低负价的代数和为2,则Y处于VA族,结合X、Y、Z的原子序数依次增大,可推知Y为N元素、Z为Na元素.
(1)钠离子结构示意图为: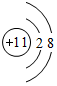 ,
,
故答案为: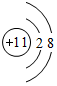 ;
;
(2)X和Y组成的化合物Q中,既含有极性共价键又含有非极性共价键,则Q为N2H4,Q在空气中燃烧产物没有任何污染,则反应生成氮气与水,化学反应方程式为:N2H4+O2$\frac{\underline{\;点燃\;}}{\;}$N2+2H2O.Q还可将酸性工业废水中的Cr2O72-还原为Cr3+,氧化产物为常见气体,则氧化产物为氮气,反应离子方程式为:2Cr2O72-+3N2H4+16H++=4Cr3++3N2↑+14H2O,
故答案为:N2H4+O2$\frac{\underline{\;点燃\;}}{\;}$N2+2H2O;2Cr2O72-+3N2H4+16H++=4Cr3++3N2↑+14H2O;
Ⅱ.(3)双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为: ,
,
故答案为: ;
;
(4)双氧水可以将废水中的氰化物转化为无毒物同时生成NH3,其中碳元素的化合价升高,结合原子守恒和电荷守恒可知无毒的物质是碳酸氢钠,反应的离子方程式为:H2O2+CN-+H2O=HCO3-+NH3,
故答案为:H2O2+CN-+H2O=HCO3-+NH3;
(5)双氧水因具有氧化性而具有杀菌消毒能力,但是2H2O2═2H2O+O2,铁离子会加速H2O2分解,使洗涤剂失去杀菌作用,此外,三价铁离子和纯碱中的碳酸根的水解双促进,2Fe3++3CO32-+3H2O═2Fe(OH)3↓+3CO2↑,使洗涤剂失去去污能力,
答:2H2O2$\frac{\underline{\;Fe_{3}+\;}}{\;}$2H2O+O2↑,Fe3+会加速H2O2分解,使洗涤剂失去杀菌作用;2Fe3++3CO32-+3H2O═2Fe(OH)3↓+3CO2↑,Fe3+与CO32-水解相互促进,使洗涤剂失去去污能力.
点评 本题属于拼合型题目,涉及元素推断、常用化学用语、氧化还原反应、陌生方程式书写、盐类水解等,侧重考查学生对题目信息的获取与知识迁移运用,试题有利于培养学生的综合能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,92 g NO2和N2O4混合气体含有的原子数为6 NA | |
| B. | 5.6 g金属铁与足量稀盐酸反应,失去的电子数为0.3 NA | |
| C. | 标准状况下,ll.2 LSO3含有的分子数为0.5 NA | |
| D. | 25℃、101 kPa时,64 g SO2中含有的氧原子数为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③⑤ | C. | ①和④ | D. | ③和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| C. | 硝酸银溶液中加入铜粉:2Ag++Cu═Cu2++2Ag↓ | |
| D. | 盐酸跟氢氧化镁反应:H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
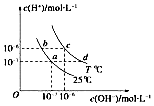
| A. | 若从a点到c点,可采用在水中加入酸的方法 | |
| B. | b点对应的醋酸中由水电离的c(H+)=10-6mol•L-1 | |
| C. | T℃时,0.05 mol•L-1的Ba(OH)2溶液的pH=11 | |
| D. | c点对应溶液的Kw大于d点对应溶液的Kw |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
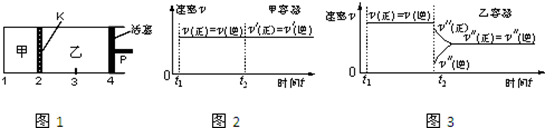
| A. | 保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
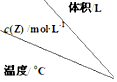 | 1 | 2 | 3 |
| 200 | $\frac{8}{3}$ | $\frac{4}{3}$ | $\frac{8}{9}$ |
| 300 | 2.4 | 1.2 | 0.8 |
| 400 | 2.0 | 1.0 | $\frac{2}{3}$ |
| A. | m=2,△H>0 | |
| B. | 300℃时,该反应平衡常数 K=9 | |
| C. | 在3L容器中进行反应,达到平衡的时间:400℃>200℃ | |
| D. | 200℃,2L容器中反应达平衡后,再充入2 mol Z,平衡时 Z 的体积分数增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com