
| A、凡是中心原子采取sp3杂化的分子,其立体构形都是正四面体 |
| B、杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
| C、CH4分子中的sp3杂化轨道是由4个H的1s轨道和C原子的2p轨道混合起来而形成的 |
| D、凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 |
| 1 |
| 2 |
| 1 |
| 2 |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
| A、pH=0的溶液不存在 |
| B、中性溶液的pH不一定等于7 |
| C、使用广泛pH试纸测得某溶液的pH=3.5 |
| D、酸或碱溶液在稀释时,溶液的pH均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2+H2O=H2CO3 化合反应 |
| B、H2CO3=CO2↑+H2O 分解反应 |
| C、3CO+Fe2O3=2Fe+3CO2 置换反应 |
| D、CuO+H2=Cu+H2O氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液 | B、蒸馏 | C、过滤 | D、蒸发 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=2的硝酸和pH=12的Ba(OH)2溶液 |
| B、pH=3的盐酸和pH=11的氨水 |
| C、pH=3的硫酸和pH=11的KOH |
| D、pH=4的醋酸和pH=10的KOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
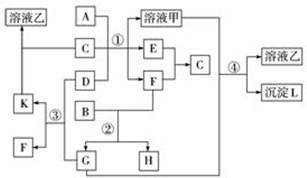 在图中表示的是有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略.)
在图中表示的是有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略.)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com