
【题目】(6分)(1)25℃时,相同物质的量浓度的下列溶液中:①NaCl ②NaOH ③ H2SO4 ④(NH4)2SO4,其中水的电离程度由大到小顺序(用序号填空):____________
(2)LiH可作飞船的燃料,已知下列反应:
① 2Li(s)+H2(g)=2LiH(s) △H=-182kJ·mol-1
②2H2(g)+O2(g)═2H2O(1)△H=-572kJ·mol-1;
③4Li(s)+O2(g)═2Li2O(s)△H=-1196kJ·mol-1
试写出LiH在O2中燃烧的热化学方程式_________。
(3)2Al+Fe2O3![]() 2Fe+Al2O3反应的△S____0(选填“>”“<”或“=”),在高温下,该反应_______(填“能”或“不能”自发进行)。
2Fe+Al2O3反应的△S____0(选填“>”“<”或“=”),在高温下,该反应_______(填“能”或“不能”自发进行)。
【答案】(1)④>①>②>③;(2)2LiH(s)+O2(g)═Li2O(S)+H2O(l)△H=-702 kJ·mol-1;
(3)=;能。
【解析】
试题分析:(1)①NaCl是强酸强碱盐,对水的电离平衡无影响; ②NaOH是一元强碱,电离产生的OH-对水的电离平衡起抑制作用,使水的电离程度减小; ③H2SO4是二元强酸,电离产生的氢离子对水的电离平衡起抑制作用,由于等浓度的氢离子、氢氧根离子对水电离平衡的抑制作用相等,则由于硫酸电离产生的氢离子浓度大于等浓度的氢氧化钠产生的氢氧根离子,所以水的电离程度比氢氧化钠小; ④(NH4)2SO4是强酸弱碱盐,NH4+会消耗水电离产生的氢氧根离子,产生弱碱,使水向电离的方向移动,最终使水的电离程度增大,故水的电离程度由大到小顺序是④>①>②>③;(2)依据热化学方程式结合盖斯定律③-①×2+②得到: 4LiH(s)+2O2(g)=2Li2O(s)+2H2O(l)△H=-1404KJ/mol,即热化学方程式为2LiH(s)+O2(g)═Li2O(s)+H2O(l)△H=-702 kJ·mol-1;(3)2Al+Fe2O3![]() 2Fe+Al2O3反应的反应物生成物都是固体,所以体系的混合程度不变,故△S=0,由于反应物的能量比生成物的能量高,该反应是放热反应,所以在高温下,该反应能自发进行。
2Fe+Al2O3反应的反应物生成物都是固体,所以体系的混合程度不变,故△S=0,由于反应物的能量比生成物的能量高,该反应是放热反应,所以在高温下,该反应能自发进行。


科目:高中化学 来源: 题型:
【题目】在“绿色化学工艺”中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%。下列反应类型能体现“原子经济性”原则的是:①置换反应 ②化合反应 ③分解反应 ④取代反应 ⑤加成反应 ⑥消去反应 ⑦加聚反应 ⑧缩聚反应
A.①②⑤ B.②⑤⑦ C.⑦⑧ D.⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有NaBr 、KI的混合溶液中通入过量的Cl2充分反应。将溶液蒸干,并灼烧所得的物质,最后剩余的固体物质是( )
A. NaCl 和KI B. NaCl、KCl和I2
C. KCl和NaBr D. KCl和NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是
A. 标准状况下,22.4LH2O含有的分子数为NA
B. 常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA
C. 通常状况下,NA个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是( )
A.25℃时,饱和KCl溶液的浓度大于4.0 mol·L-1
B.此溶液中KCl的质量分数为![]() ×100%
×100%
C. 20℃时,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174 g·cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A的红外光谱和核磁共振氢谱图如图所示,下列说法中错误的是( )

A.由红外光谱可知,该有机物中至少有三种不同的化学键
B.若A的化学式为C2H6O,则其结构简式为CH3﹣O﹣CH3
C.仅由其核磁共振氢谱图无法得知其分子中的氢原子总数
D.由核磁共振氢谱图可知,该有机物分子中有三种不同的氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设汁下列实验方案鉴别Na2CO3和NaHC03两种白色粉末,不能达到预期目的是( )
A. 分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
B. 分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少
C. 分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
D. 分别将等量的白色粉末用如图所示装置进行实验,比较澄清石灰水是否变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知图一表示的是可逆反应CO(g)+H2(g)![]() C(s)+H20(g) △H >0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)
C(s)+H20(g) △H >0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)![]() N2O4(g) △H<0 的浓度(c)随时间t的变化情况。下列说法中正确的是( )
N2O4(g) △H<0 的浓度(c)随时间t的变化情况。下列说法中正确的是( )
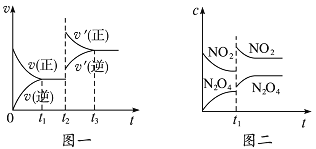
A. 图一t2时改变的条件可能是升高了温度或增大了压强
B. 若图一t2时改变的条件是增大压强,则反应的△H增大
C. 图二t1时改变的条件可能是升高了温度或增大了压强
D. 若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学式与俗名相符的是
A. 小苏打Na2CO3,苛性钠NaOH
B. 芒硝Na2SO4·10H2O,消石灰Ca(OH)2
C. 苏打NaHCO3,石灰石CaCO3
D. 纯碱NaOH,食盐NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com