
【题目】常温下,向10.00 mL 0.1mol/L某二元酸H2X溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化如图所示(忽略温度变化),已知:常温下,H2X的电离常数Ka1=1.1×10-5,Ka2=1.3×10-8。下列叙述正确的是

A.a近似等于3
B.点②处c(Na+)+2c(H+)+c(H2X)=2c(X2-)+c(HX-)+2c(OH-)
C.点③处为H2X和NaOH中和反应的滴定终点
D.点④处c(Na+)=2c(X2-)>c(OH-)>c(HX-)>c(H+)
【答案】A
【解析】
A.多元弱酸分步电离,以第一步为主,根据H2X![]() H++HX-,c(H+)=
H++HX-,c(H+)=![]() =
=![]() ≈10-3,a近似等于3,故A正确;
≈10-3,a近似等于3,故A正确;
B.点②处恰好生成NaHX,根据电荷守恒c(Na+)+c(H+)=2c(X2-)+c(HX-)+c(OH-)和质子守恒c(H+)+c(H2X)= c(X2-)+c(OH-)得:c(Na+)+2c(H+)+ c(H2X)=3 c(X2-)+ c(HX-)+2c(OH-),故B错误;
C. H2X和NaOH恰好反应生成Na2S,为中和反应的滴定终点,点④处为滴定终点,故C错误;
D.点④处恰好生成Na2X,c(Na+)>2c(X2-)>c(OH-)>c(HX-)>c(H+),故D错误;
答案:A


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】利用氨气脱硝![]() 除
除![]() 是大气污染防治研究的热点,脱硝过程中涉及的反应为:
是大气污染防治研究的热点,脱硝过程中涉及的反应为:
主反应:![]()
副反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905.5KJ/mol
②4NH3(g)+4O2(g)=2N2O(g)+6H2O(g) △H=-1104.9KJ/mol
③4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-1269.0KJ/mol
回答下列问题:
(1)主反应的△H为______
(2)如图所示,保持其它条件相同,使用两种不同的催化剂,主反应NO的转化率与温度关系如图所示:
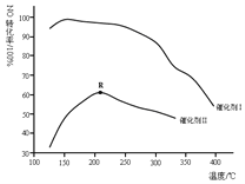
①选用催化剂I的优势有______![]() 写出一点
写出一点![]()
②R点对应的温度为2100C,低于2100C,NO的转化率是不是对应温度下的平衡转化率,请作出判断并写出理由______.
(3)常温下,在通入氧气的条件下用![]() 的NaOH溶液吸收NO也可实现脱硝
的NaOH溶液吸收NO也可实现脱硝![]() 产物主要为
产物主要为![]() 和
和![]() ,已知反应后溶液的
,已知反应后溶液的![]() ,溶液中
,溶液中![]() 浓度为5.6×10-2mol/L,忽略反应过程中溶液体积变化,
浓度为5.6×10-2mol/L,忽略反应过程中溶液体积变化,![]() 的电离平衡常数为5.1×10-4,则:
的电离平衡常数为5.1×10-4,则:
①c(NO2-)c(OH-)/c(HNO2)=______![]()
②某溶液中c(NO2-)=1.0×10-6mol/L,取该溶液5mL,加入一滴![]() 的硝酸银溶液
的硝酸银溶液![]() 一滴为
一滴为![]() ,通过计算说明能否产生沉淀______[Ksp(AgNO2)=2×10-8]
,通过计算说明能否产生沉淀______[Ksp(AgNO2)=2×10-8]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体电解质有广泛的用途。研究发现,晶体中有特殊结构为离子![]() 如
如![]() 提供快速迁移的宽敞通道或者有“点缺陷”,都能使其具有导电潜力。比如:图
提供快速迁移的宽敞通道或者有“点缺陷”,都能使其具有导电潜力。比如:图![]() 所示的锂超离子导体
所示的锂超离子导体![]() 和图
和图![]() 所示的有“点缺陷”的NaCl。
所示的有“点缺陷”的NaCl。
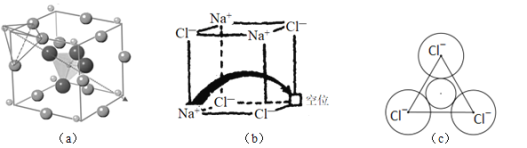
根据所学知识回答下列问题:
(1)在变化“Cl+e-→Cl-”过程中,所得电子填充在基态Cl的________能级,此过程会_______![]() 填“吸收”或“释放”
填“吸收”或“释放”![]() 能量。
能量。
(2)![]() 中B的杂化形式为__________,其等电子体为:___________
中B的杂化形式为__________,其等电子体为:___________![]() 任写一种
任写一种![]() 。与其VSEPR模型相同,且有1对孤电子对的相对分子质量最小的分子是____________。
。与其VSEPR模型相同,且有1对孤电子对的相对分子质量最小的分子是____________。
(3)图![]() 所示晶胞中
所示晶胞中![]() 位于__________位置;若将晶体中形成宽敞通道的
位于__________位置;若将晶体中形成宽敞通道的![]() 换成
换成![]() ,导电能力会明显降低,原因是_____________。
,导电能力会明显降低,原因是_____________。
(4)图![]() 中,若缺陷处填充了
中,若缺陷处填充了![]() ,则它____________
,则它____________![]() 填“是”或“不是”
填“是”或“不是”![]() 的晶胞,在NaCl晶体中,
的晶胞,在NaCl晶体中,![]() 填充在
填充在![]() 堆积而成的___________面体空隙中。
堆积而成的___________面体空隙中。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法正确的组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、H2O、H2S晶体的熔点依次降低
④离子化合物中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2-相紧邻
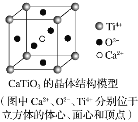
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠溶于水时离子键被破坏
A. ①②③⑥B. ①②④C. ③⑤⑦D. ③⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COCl2(g)![]() CO(g) + Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2 分解率的是
CO(g) + Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2 分解率的是
A.①④⑥B.①②④C.②③⑥D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光纤通讯是光导纤维传送信号的一种通讯手段,合成光导纤维及氮化硅(一种无机涂层)的工艺流程如下:

回答下列问题:
(1)反应I的化学方程式为2C+SiO2![]() Si+2CO↑,其中还原剂为_______________,产物Si在周期表中位于_______________,该反应涉及的副反应可能有C+SiO2
Si+2CO↑,其中还原剂为_______________,产物Si在周期表中位于_______________,该反应涉及的副反应可能有C+SiO2![]() Si+CO2↑(碳不足)和__________________________________(碳足量)。
Si+CO2↑(碳不足)和__________________________________(碳足量)。
(2)经反应Ⅱ所得的四氯化硅粗品中所含的物质如下:
组分名称 | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
质量分数 | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
沸点/℃ | 57.6 | 31.8 | 8.2 | -85 | 12.5 | 75.5 |
图中“操作X”的名称为______________________;PCl3的电子式为________________。
(3)反应IV的化学方程式为SiCl4+4NH3![]() Si3N4+12HCl,若向一2L恒容密闭容器中投入1molSiCl4和1molNH3,6min后反应完全,则0~6min内,HCl的平均反应速率为__________mol/(L·min)。反应III的与IV产生的气体相同,则反应III化学方程式为__________________。反应III中的原料气H2和O2在碱性条件下可构成燃料电池,其正极反应的电极方程式为__________________。
Si3N4+12HCl,若向一2L恒容密闭容器中投入1molSiCl4和1molNH3,6min后反应完全,则0~6min内,HCl的平均反应速率为__________mol/(L·min)。反应III的与IV产生的气体相同,则反应III化学方程式为__________________。反应III中的原料气H2和O2在碱性条件下可构成燃料电池,其正极反应的电极方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,实验测得1.0 mol·L-1 NH4HCO3溶液的 pH=8.0。平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示。下列说法正确的是

A. 常温下Ka1(H2CO3)>Kb(NH3·H2O)>Ka2(H2CO3)
B. pH=13时,溶液中不存在![]() 的水解平衡
的水解平衡
C. pH由8~11时, ![]() 不变
不变
D. pH=3时,有c(![]() )+c(NH3·H2O)=c(
)+c(NH3·H2O)=c(![]() )+c(
)+c(![]() )+c(H2CO3)
)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火力发电厂释放出大量氮氧化合物(NOx)、SO2和CO2等气体会造成环境问题。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+ 4NO2(g)=4NO(g)+ CO2(g)+ 2H2O(g) △H1=-574 kJ/mol
CH4(g)+ 4NO(g)=2N2(g)+ CO2(g)+ 2H2O(g) △H2=-1160 kJ/mol
甲烷直接将NO2还原为N2的热化学方程式为___________。
(2)脱碳。将CO2转化为甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
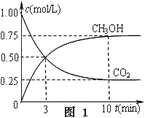

①在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如图1所示。回答:0~10 min内,氢气的平均反应速率为___mol/(L·min);第10 min后,保持温度不变,向该密闭容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡________(填“正向”、“逆向”或“不”)移动。
②如图2,25℃时以甲醇燃料电池(电解质溶液为稀硫酸)为电源来电解300mL 某NaCl溶液,正极反应式为______。在电解一段时间后,NaCl溶液的pH值变为13(假设NaCl溶液的体积不变),则理论上消耗甲醇的物质的量为_____mol。
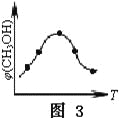
③取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图3所示,则上述CO2转化为甲醇的反应的△H3____0(填“>”、“<”或“=”)。
(3)脱硫。燃煤废气经脱硝、脱碳后,与一定量氨气、空气反应,生成硫酸铵。硫酸铵水溶液呈酸性的原因是______(用离子方程式表示);室温时,向(NH4)2SO4,溶液中滴人NaOH溶液至溶液呈中性,则所得溶液中微粒浓度大小关系c(Na+)_____c(NH3·H2O)。(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是

A. 向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B. 实验中装置b中的液体逐渐变为浅红色
C. 装置c中的碳酸钠溶液的作用是吸收溴化氢
D. 反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com