
【题目】工业电解饱和食盐水产生的氯气制漂白粉,所进行的反应是
① 2NaCl+2H2O![]() Cl2+H2+2NaOH
Cl2+H2+2NaOH
② 2Ca(OH)2(石灰乳)+ 2Cl2 =CaCl2+Ca(ClO)2+2H2O
某厂日产漂白粉(含量80%,主要杂质Ca(OH)2)20吨,已知进行①步反应的转化率90%,进行②步转化率85%。
(1)写出②反应的离子方程式并用双线桥标出电子转移数目
(2)列式计算该厂日消耗精制后的NaCl多少摩尔?(科学计数值,保留小数点后两位)
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是人类获取能量的重要途径。
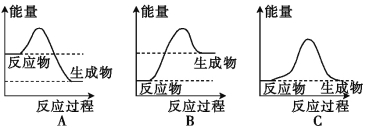
(1)液化气是一种重要的家用燃料,下列示意图与液化气在燃烧过程中的能量变化最相符的是 (填字母)。
(2)“冰袋”可用于短时间保鲜食物。将一定量的碳酸钠晶体与硝酸铵晶体密封于一塑料袋中,用线绳绑住塑料袋中间部分,使两种晶体隔开,做成“冰袋”。使用时将线绳解下,用手将袋内两种固体粉末充分混合,便立即产生低温。由此判断:碳酸钠晶体与硝酸铵晶体的总能量 (填“高于”或“低于”)反应后生成产物的总能量。
(3)化学反应中的能量变化不仅仅表现为热量的变化,有时还可以表现为其他形式的能量变化。比如,蜡烛燃烧可用来照明,这个过程是将化学能转化为 和 ;人们普遍使用的干电池工作时是将化学能转化为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SiO2俗称石英砂,是光导纤维的主要成分,下列关于SiO2的有关叙述正确的是
A. SiO2是酸性氧化物,它不溶于水也不溶于任何酸
B. SiO2是制造玻璃的主要原料之一,它在常温下不与NaOH溶液反应
C. 因高温时SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3的强
D. CO2通入水玻璃中可得硅酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品卫生与人们的身体健康密切相关,下列做法符合《食品卫生法》的是
A.用工业用盐腌制咸菜 B.在牛奶中添加尿素
C.用二氧化硫熏制银耳 D.用纯碱发酵面食
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的的是
A. 用点燃的方法除去CO2中少量的CO
B. 在蒸发皿中蒸发氯化镁溶液制备无水氯化镁
C. 室温下测定等浓度的醋酸和盐酸的pH比较二者酸性强弱
D. 用酸性高锰酸钾溶液检验氯化亚铁溶液中的亚铁离子是否存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下.NH4Cl溶液加水稀释,![]() 增大
增大
B.0.1mol/LNa2CO3溶液加热后,溶液的pH减小
C室温下稀释0.1mol/LCH3COOH溶液,溶液的导电能力减弱,因此溶液中所有离子浓度均减小
D.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进Fe3+水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。

请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是_________________,滤渣A的主要成分是_______________。
(2)下列物质中最适合的氧化剂B是________;反应的离子方程式 。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲、乙的名称分别是:甲______________,乙___________________。
(4)上述流程中,氧化之后和加热蒸发之前,需取少量溶液检验Fe2+是否已全部被氧化,所加试剂 能否用酸性的KMnO4溶液? (填“能”或“不能”)理由是: 。(可用语言或方程式说明)
(5)检验硫酸铁铵中NH4+的方法是____________________________。
(6)称取14.00 g样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba (NO3) 2溶液,恰好完全反应。则该硫酸铁铵的化学式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
A.我国目前使用的主要能源是化石能源
B.氢能源的优点有:热量值高、对环境友好
C.核能发电是解决能源危机的最佳途径
D.太阳能的缺点有:能量密度低、稳定性差
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com