
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,四种元素同周期,X的金属性在同周期元素中最强;Y原子的电子层数与最外层电子数相等;Z元素在地壳中的含量居于第二位;W的最高价氧化物的水化物的化学式为HnWO2n+2。下列说法正确的是( )
A.简单离子半径:X<Y<W
B.Y、Z两种元素的氧化物均具有两性
C.X、W分别形成的氢化物中所含化学键种类相同
D.Z、W形成化合物的电子式为:
【答案】D
【解析】
四种元素同周期,X的金属性在同周期元素中最强,X为Na元素;Z元素在地壳中的含量居于第二位,Z为Si;W的最高价氧化物的水化物的化学式为HnWO2n+2,当n=1时,该酸为HClO4,所以W为Cl;Y原子的电子层数与最外层电子数相等。所以Y为Al。
结合以上分析可知:X、Y、Z、W分别为Na、Al、Si、Cl;
A.核外电子排布相同的离子,核电荷数越大,离子半径越小,简单离子半径![]() ,A错误;
,A错误;
B.![]() 是酸性氧化物,与碱反应生成盐和水,无两性,B错误;
是酸性氧化物,与碱反应生成盐和水,无两性,B错误;
C.NaH为离子化合物,含离子键,HCl为共价化合物,含共价键,C错误;
D.![]() 为含有4对共用电子对的共价化合物,氯原子、硅原子最外层均达到8电子稳定结构,电子式书写正确,故D正确;
为含有4对共用电子对的共价化合物,氯原子、硅原子最外层均达到8电子稳定结构,电子式书写正确,故D正确;
答案选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 四种短周期元素在元素周期表中的相对位置如图所示,这四种元素原子的最外层电子数之和为20。下列判断正确的是
四种短周期元素在元素周期表中的相对位置如图所示,这四种元素原子的最外层电子数之和为20。下列判断正确的是
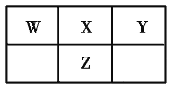
A.四种元素的原子半径:![]()
B.四种元素形成的单质最多有6种
C.四种元素原子均可与氢原子形成电子总数为18的分子
D.![]() 与
与![]() 可形成离子化合物
可形成离子化合物![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炭循环(如图)对人类生存、发展有着重要的意义,下列说法错误的是
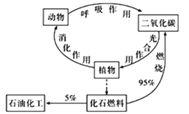
A.碳是组成有机物的主要元素
B.光合作用是将太阳能转化为化学能的过程
C.动物呼吸产生CO2的过程中,葡萄糖被氧化
D.碳元素在地壳中含量丰富,因此其形成的化合物数量众多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】画出下列元素的原子结构示意图:
(1)质量数为23,中子数为12的原子:________。
(2)某元素原子的最外层电子数等于次外层电子数:__________________。
(3)某元素的原子L层电子数是M层电子数的2倍:__________________。
(4)某原子核内没有中子的元素:________。
(5)电子总数是最外层电子数3倍的原子________。
(6)某元素原子的最外层电子数等于次外层电子数的2倍:________。
(7)某元素原子L层上的电子数为K层的3倍:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光气是一种重要的有机中间体,在农药、医药、工程塑料、聚氨酯材料以及军事上都有许多用途。光气很容易水解,熔点为-118°C,沸点为8.2°C。某科研小组模拟工业生产由一氧化碳和氯气的混合物在活性炭作催化剂的条件下制取光气,其反应原理为:Cl2+CO=COCl2。装置如图所示(丙处的加油装置已省略,D中仪器用于收集光气)。
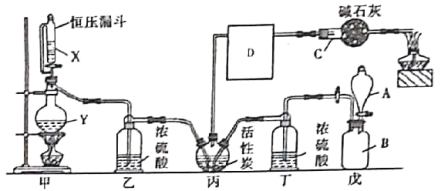
(1)仪器C的名称为___,其中碱石灰的作用为________________,D中仪器应浸在_____(填“冰水浴”或“热水浴”)中。
(2)仪器组装完成后,检验甲装置气密性的方法是_________。
(3)戊装置主要用于制取氯气,用酸性KMnO4和盐酸制取氯气时的离子方程式为__________。
(4)光气极易水解,遇水后易产生一种氢化物和一种氧化物,其反应的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制取Na2CO3和高纯Si的工艺流程如图所示,下列说法错误的是
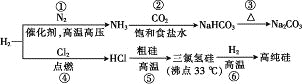
A. 反应①属于固氮反应
B. 步骤②为先向饱和食盐水中通入CO2至饱和后,再通入NH3
C. 反应⑤、⑥均为氧化还原反应
D. 用精馏的方法可提纯三氯氢硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硅酸盐的说法正确的是( )
A.硅酸盐中的阴离子都是![]()
B.硅酸盐都难溶于水
C.通常用氧化物的形式表示硅酸盐的组成,说明硅酸盐就是由各种氧化物组成的
D.![]() 是一种简单的硅酸盐,其水溶液可用作黏合剂
是一种简单的硅酸盐,其水溶液可用作黏合剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A是近年来采用的锅炉水添加剂,其结构式如图,A能除去锅炉水中溶解的氧气,下列说法正确的是( )
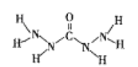
A. A分子中所有原子都在同一平面内
B. A分子中所含的σ键与π键个数之比为10:1
C. 所含C、N均为sp2杂化
D. A与O2反应生成CO2、N2、H2O的物质的量之比为1:2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA为阿伏加德罗常数)( )
A. 12 g石墨中含有C—C键的个数为1.5 NA
B. 12 g金刚石中含有C—C键的个数为4 NA
C. 60 g SiO2中含有Si—O键的个数为2 NA
D. 124 g P4中含有P—P键的个数为4 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com