
分析 (1)CH4和澄清石灰水及浓硫酸都不反应,所以最后得到的气体是CH4,n(CH4)=$\frac{14L}{22.4L/mol}$=0.625mol,
根据m=nM计算甲烷质量;
(2)二氧化碳和澄清石灰水反应生成CaCO3,则得到的白色沉淀是碳酸钙,根据C原子守恒得n(CO2)=n(CaCO3)=$\frac{20g}{100g/mol}$=0.2mol;
(3)根据C原子守恒得n(C)=n(CH4)+n((CO2)=0.625mol+0.2mol=0.825mol,根据N=nNA计算C原子数目.
解答 解:(1)CH4和澄清石灰水及浓硫酸都不反应,所以最后得到的气体是CH4,n(CH4)=$\frac{14L}{22.4L/mol}$=0.625mol,
m(CH4)=nM=0.625mol×16g/mol=10g,
故答案为:10g;
(2)二氧化碳和澄清石灰水反应生成CaCO3,则得到的白色沉淀是碳酸钙,根据C原子守恒得n(CO2)=n(CaCO3)=$\frac{20g}{100g/mol}$=0.2mol,n(CH4)=0.625mol,所以原混合气体中CH4的物质的量比CO2多0.625mol-0.2mol=0.425mol,故答案为:0.425;
(3)根据C原子守恒得n(C)=n(CH4)+n((CO2)=0.625mol+0.2mol=0.825mol,N(C)=nNA=0.825mol×NA/mol=0.825NA,
故答案为:0.825NA.
点评 本题考查混合物的计算,为高频考点,侧重考查学生分析计算能力,把握物质的量有关公式及原子守恒的正确运用是解本题关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
 (2)H2H:H(3)MgCl2
(2)H2H:H(3)MgCl2
 (5)CO2
(5)CO2 (6)Na2O
(6)Na2O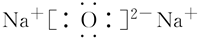
 ;O=C=O.
;O=C=O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu和足量的稀硝酸反应产生4.48 L气体时,转移的电子数为0.6×6.02×1023 | |
| B. | 常温常压下,8.8 g CO2和N2O混合物中所含有的原子总数为0.6×6.02×1023 | |
| C. | 标准状况下,3.36 L己烷中含有的分子数目为0.15×6.02×1023 | |
| D. | 在1 L 0.2 mol/L的硫酸铁溶液中含有的三价铁离子数为0.4×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
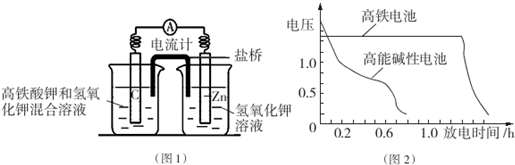
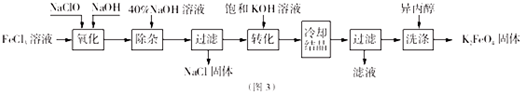
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与硫酸混合:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 铁粉与硝酸银溶液反应:Fe+2Ag+═Fe2++2Ag | |
| C. | 氯化铝溶液与过量的氨水反应:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com