
【题目】只给出下列甲中和乙中对应的量,不能组成一个求物质的量的公式的是

A.③ B.③④ C.②③④ D.③④⑤
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )

A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol 电子
3H2+CO,每消耗1molCH4转移12mol 电子
B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C. 电池工作时,CO32-向电极B移动
D. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计实验,测定Na2CO3与NaHCO3混合物中Na2CO3的质量分数。
甲方案:
实验步骤为:①称量空坩埚的质量为A g
②称量装有试样的坩埚质量为B g ③加热
④冷却⑤称量坩埚和残余物的质量为C g
⑥重复③至⑤操作,直至恒重,质量为D g
(1)坩埚中发生反应的化学方程式为__________________。
(2)计算Na2CO3质量分数必须用到的测定数据为___________(填“A”、“B”、“C”或“D”)。
乙方案:
在天平上准确称取0.3000 g样品,放入锥形瓶中,加入适量水溶解,滴入2滴酚酞试液,用0.1000 mo1·L-1,的标准盐酸滴定至溶液由粉红色刚好变为无色,达到滴定终点时产物为NaHCO3。重复上述操作两次,消耗盐酸的体积为20.00 mL。
(3)配制上述盐酸标准溶液100 mL,若用2.0 mol·L-1HCl进行配制,需用滴定管量取该HCl溶液________mL;定容时俯视刻度线,将导致配制的溶液浓度___________(填“偏高”、“偏低”或“没有影响”)。
(4)样品中Na2CO3的质量分数为___________(用百分数表示,精确到0.1%)。
丙方案:
称取m g样品,选用下图部分装置测定样品与硫酸反应生成的气体体积。
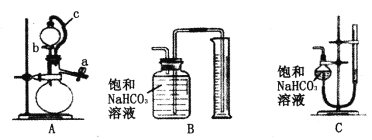
(5)某同学按以下方法检查装置A的气密性:在分液漏斗中加入适量水,如图连接好装置,关闭止水夹a,用止水夹夹住橡皮管c,打开活塞b。若装置不漏气,则观察到的现象为__________________。实验时,装置A中c的作用_____________、_____________。
(6)为了提高测定的准确性,应选用装置A和__________(填写字母标号)进行实验。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有下列十种物质:①O2;②Fe;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁胶体;⑧硫酸钠溶液;⑨稀硝酸;⑩Cu2(OH)2CO3。
(1)按物质的树状分类法填写表格的空白处:
分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 |
属于该类的物质 | ② | ⑧⑨ |
(2)上述物质中属于非电解质的有_________;上述物质中能与盐酸反应的电解质有________(填序号)。
Ⅱ.(1)在 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O 的反应中,氧化剂是_________,还原产物是_________,氧化产物与还原产物的质量比是_________。
(2)在反应MnO2+4HCl=MnCl2+Cl2↑+2H2O中,每生成标准状况下4.48LCl2,转移的电子的物质的量为___________mol。
Ⅲ.Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O组成的一个氧化还原反应体系中,发生BiO3-→Bi3+的反应过程,据此回答下列问题:
将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+ _________+ ________![]() _________+ ________+H2O
_________+ ________+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,下列叙述正确的是( )
A.1 mol NH3与1 mol OH-所含的质子数均为10NA
B.标准状况下,22.4L CHCl3中含C—H键数目为NA
C.1mol Fe与足量的稀HNO3反应时,转移3NA个电子
D.常温下,pH=13的NaOH溶液中含OH-数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某阳离子为钠离子的溶液中,可能含有SO42-、CO32-、Cl-的一种或几种,只取原溶液一次,便能一一检验其中存在的阴离子。下列加入试剂的顺序最合理的是
A. HNO3、Ba(NO3)2、AgNO3 B. Ba(NO3)2、AgNO3、HNO3
C. 酚酞、Ba(NO3)2、AgNO3 D. HCl、BaCl2、AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 2SO2(g)+O2(g)2SO3 (g)△H<0,下列说法不正确的是( )
A. 升高温度,正、逆反应速率均加快
B. 增大压强,化学平衡正向移动
C. 当气体总质量不变时,反应达平衡状态
D. 充入O2,可提高SO2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据该反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如下图所示。
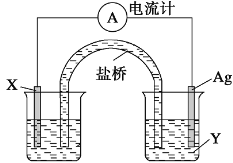
请回答下列问题:
(1) 电极X的材料是____________(写物质名称);电解质溶液Y是______________ (写化学式);
(2)银电极为电池的___________极,发生的电极反应为__________________;
X电极上发生的电极反应为_________________________________;
(3)外电路中的电子是从___________电极流向___________电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,可用离子方程式H++OH-= H2O表示的是
A.NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
B.Mg(OH)2+2HCl==MgCl2+2H2O
C.NaOH+NaHCO3==Na2CO3+H2O
D.NaOH+HNO3==NaNO3+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com