某课外活动小组同学用如图Ⅰ装置进行实验,试回答下列问题。
(1)若开始时开关K与a连接,则B极的电极反应式为_____________。
(2)若开始时开关K与b连接,则总反应的离子方程式为________________________;有关上述实验,下列说法正确的是(填序号)___________。
①溶液中Na
+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模仿工业上用离子交换膜法制烧碱的方法,设想用如图Ⅱ装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽工作时,通过阴离子交换膜的离子数_______(填“大于” “小于”或“等于”)通过阳离子交换膜的离子数。
②通电开始后,阴极附近溶液pH会增大,请简述原因_____________。
(4)多晶硅主要采用SiHCl
3还原工艺生产,其副产物SiCl
4的综合利用收到广泛关注。
①SiCl
4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl
4与H
2和O
2反应,产物有两种,化学方程式为____________________。
②SiCl
4可转化为SiHCl
3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3SiCl
4(g)+2H
2(g)+Si(s)
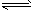
4SiHCl
3(g)达平衡后,H
2与SiHCl
3物质的量浓度分别为0.140mol/L和0.020mol/L,若H
2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为________kg。


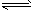 4SiHCl3(g)达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为________kg。
4SiHCl3(g)达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为________kg。  出彩同步大试卷系列答案
出彩同步大试卷系列答案 某课外活动小组同学用如图装置进行实验,试回答下列问题.
某课外活动小组同学用如图装置进行实验,试回答下列问题. (2008?东莞模拟)某课外活动小组同学用右图装置进行实验,试回答下列问题.
(2008?东莞模拟)某课外活动小组同学用右图装置进行实验,试回答下列问题. 气、氧气、硫酸和氢氧化钾.
气、氧气、硫酸和氢氧化钾. 某课外活动小组同学用右图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.
某课外活动小组同学用右图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题. 某课外活动小组同学用如图装置进行实验,试回答下列问题:
某课外活动小组同学用如图装置进行实验,试回答下列问题: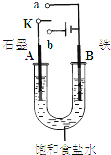 某课外活动小组同学用右图装置进行实验,试回答下列问题.
某课外活动小组同学用右图装置进行实验,试回答下列问题.