


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:021
设 为阿伏加德罗常数值,下列有关
为阿伏加德罗常数值,下列有关 硫酸钾溶液的说法中错误的是
硫酸钾溶液的说法中错误的是
[ ]
A.1L溶液中含有0.3 个
个
B.1L溶液中含有 和
和 总数为0.9
总数为0.9
C.2L溶液中 的物质的量浓度为
的物质的量浓度为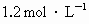
D.2L溶液中含有0.6 个
个
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:021
设 为阿伏加德罗常数值,下列有关
为阿伏加德罗常数值,下列有关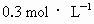 硫酸钾溶液的说法中错误的是
硫酸钾溶液的说法中错误的是
[ ]
A.1L溶液中含有0.3 个
个
B.1L溶液中含有 和
和 总数为0.9
总数为0.9
C.2L溶液中 的物质的量浓度为
的物质的量浓度为
D.2L溶液中含有0.6 个
个
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省唐山市高三第一次模拟考试理综化学试卷(解析版) 题型:推断题
已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素。试回答下列有关的问题:
(1)写出F元素的电子排布式_______。
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为______。
(3)已知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子空间构型是______。
(4)B、C、D、E的第一电离能由大到小的顺序是______ (写元素符号)。四种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是______(写化学式)。
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都有球型对称结构,它们都可以看作刚性圆球,并彼此“相切”。如下图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:

晶胞中距离一个Na+最近的Na+有____________个。若晶体密度为ρ g·cm-3,阿伏加德罗常的值用NA表示,则Cl-的离子半径_____cm(用含NA与ρ式子表达)。
查看答案和解析>>
科目:高中化学 来源:2012届山西省高二下学期期中考试化学试卷 题型:填空题
(15分)下表是长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是 (填编号)。
(2)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为 (用对应的元素符号表示)。

(3)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是 。
a.分子中含有氢键 b.属于非极性分子
c.含有4个σ键和1个π键 d.该氢化物分子中,②原子采用sp2杂化
(4)某元素的外围电子排布式为nsnnpn+1,该元素可与①形成三角锥形的分子X, X在①与③形成的分子Y中的溶解度很大,其主要原因是
。
(5)将过量的X通入含有元素⑩的硫酸盐溶液中,现象是 ,反应的离子方程式_ 。
(6) ⑩单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.

若已知⑩的原子半径为d,NA代表阿伏加德罗常数,⑩的相对原子质量为M,请回答:晶胞中⑩原子的配位数为________,该晶体的密度为___ _____(用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08上海建平中学期末)设2N A为阿伏加德罗常数值,下列有关叙述不正确的是 ( )
A.常温常压下,lmol甲基(一CH3)所含的电子数为10 N A
B.0.4mol以任意比例混合的乙炔和乙醛混合气体,在氧气中充分燃烧。消耗氧气的分子数为N A
C.常温常压下,N A个甲烷分子的体积大于22.4L
D.O.1molK2O2与水反应时,转移的电子数为2N A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com