
锌(Zinc)是第四“常见”的金属,仅次于铁、铝及铜,在现代工业中对于电池制造有不可磨灭的贡献。
Ⅰ.湿法炼锌
某种冶炼过程可用下图简略表示
(1)ZnS焙烧反应的化学方程式为___________________________________。
(2)电解过程中析锌一极的电极反应式为_____________________________。
(3)氧化锌像氧化铝一样,属于两性氧化物,则氧化锌与氢氧化钠反应的离子方程式为_______________________________________________________。
(已知:“锌酸”的化学式可写成H2[Zn(OH)4])
Ⅱ.锌电池
用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等。
(4)锌锰碱性电池,以二氧化锰为正极,锌粒为负极,氢氧化钾溶液为电解液。其具有容量大、放电电流大的特点,因而得到广泛应用。电池总反应式为Zn+2MnO2+2H2O===2MnO(OH)+Zn(OH)2。
碱性电池中,负极锌由片状改变成粒状的优点是__________________________;正极反应式为________________________
(5)新型锌空电池(如图)与锂电池相比,锌空气充电电池的储存电量是它的三倍,成本是锂电池的一半,并且完全没有过热爆炸的安全隐患。该电池的总反应为2Zn+O2===2ZnO,电解质溶液为KOH溶液,则负极的电极反应式为________________________________________。
若以该电池为电源,用惰性电极电解硝酸银溶液,为保证阴极有10.8 g银析出,至少需要________L空气(折算成标准状况)进入该电池。
科目:高中化学 来源: 题型:填空题
市场上出售的“热敷袋”的主要成分是铁屑、炭粉、木屑、少量氯化钠和水等。“热敷袋”启用之前用塑料袋使其与空气隔绝,启用时,打开塑料袋轻轻揉搓就会放出热量,使用完后,会发现有大量铁锈存在。
(1)热敷袋是利用________放出热量。
(2)炭粉的主要作用是__________________________________。
(3)加入氯化钠的主要作用是____________________________。
(4)木屑的作用是______________________________________。
(5)有关的电极反应式和化学方程式是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解
质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液的电解实验,如图所示。
回答下列问题:
(1)甲烷燃料电池正极的电极反应式为 、负极的电极反应式为 。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠溶液的化学方程式为 ;若电解一段时间后,石墨棒上产生标准状况下的Cl2 224 mL,电解后的溶液总体积为200 mL,则溶液的pH = 。
(3)若每个电池甲烷通入量为 1 L(标准状况),且反应完全,则理论上通过电解池的电量为 (法拉第常数F = 9.65×l04C· mol-1,列式计算),最多能产生的氯气体积为 L (标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
电解是最强有力的氧化还原手段,在化工生产中有着重要的应用。请回答下列问题:
(1)以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为________,阴极反应式为________。
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是
___________________________________________________(填序号)。
a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH
实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入________(填化学式),电极反应式为________。电解过程中,阴极区Na2SO4的物质的量________(填“增大”、“减小”或“不变”)。
②在实际工艺处理中,阴极区乙醛的去除率可达60%。若在两极区分别注入1 m3乙醛含量为3 000 mg/L的废水,可得到乙醇________kg(计算结果保留小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
海洋资源的开发与利用具有广阔的前景。海水的pH一般在7.5~8.6之间。某地海水中主要离子的含量如下表:
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | S | HC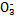 |
| 含量/(mg·L-1) | 9 360 | 83 | 200 | 1 100 | 16 000 | 1 200 | 118 |
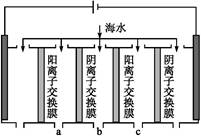
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
微电解技术具有处理效果显著、投资少、运行费用低等优点。铝碳微电解处理就是利用铝-碳颗粒之间形成了无数个细微原电池,这些细微电池在酸性溶液中发生电化学反应。溶液中溶解一定量的氧可以增大铝的腐蚀效率,因此可以通过曝气来强化处理效果。实验装置如图:
(1)实验前,将铝屑在5%NaOH碱洗10分钟,目的是① ,② 。
(2)曝气条件下,在酸性溶液中,该装置中发生的电极反应为:铝极 ,碳极 。
(3)通过铝碳微电解法可以对含镍电镀废水进行处理,某化学研究小组研究了铝碳比、反应停留时间对处理效果的影响,结果如下:

通过分析,确定最佳工艺的铝碳比为 ,反应停留时间是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
迄今为止,由化学能转变的热能或电能仍然是人类使用的主要的能源。
I.请仔细观察下列两种电池的构造示意图,完成下列问题:
(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是 。
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式为 。
Ⅱ.下面是一个将化学能与电能相互转化的装置。回答下列问题:
(1)写出通入O2一极的电极反应方程式为 。
(2)a电极是 极,能否写出其电极反应方程式 (填“能”或“不能”),若“能”写出其电极反应方程式,若“不能”说明其理由 。
(3)下列说法不正确的是( )
| A.此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变 |
| B.U型管中,OH—在a极放电 |
| C.若a为纯净金属,b为粗制金属,该装置可用于粗制金属的精炼 |
| D.电子经导线流入b电极 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)乙酰水杨酸俗称阿司匹林,是一种历史悠久的解热镇痛药。乙酰水杨酸的结构简式为 。
。
现有乙酰水杨酸的粗品,某同学用中和法测定产品纯度:取a g产品溶解于V1 mL1mol/L的NaOH溶液中,加热使乙酰水杨酸水解,再用1 mol/L的盐酸滴定过量的NaOH,当滴定终点时消耗盐酸V2 mL;
①写出乙酰水杨酸与NaOH溶液反应的化学方程式 ;
②计算出产品纯度为 (只需列出计算表达式,不必化简。乙酰水杨酸相对分子质量为180)。
(2)甲醇直接燃料电池具有启动快、效率高、能量密度高等优点。(已知二甲醚直接燃料电池能量密度E =8.39 kW·h·kg-1)。
①若电解质为酸性,甲醇直接燃料电池的负极反应为 ;
②该电池的理论输出电压为1.20 V,能量密度E = (列式计算。能量密度 = 电池输出电能/燃料质量,lkW·h = 3.6×106J,一个电子的电量=1.6×10-19C)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题:
(1)打开K2,闭合K1,B为_______极,A的电极反应为_____,最终可观察到的现象是 。
(2)打开K1,闭合K2,E为_______极,检验F极产生气体的方法是 。该装置中发生反应的化学方程式为_________。
(3)若往U型管中滴加酚酞,进行(1)、(2)操作时, 极周围能变红(填A、B、E、或F)。
(4)若电源选用燃料电池,结构如下图,以熔融碳酸盐为电解质(非水溶济,能够传导CO32-),电池工作时电解质组成保持稳定,通入甲烷的电极为________极,请写出正极反应的方程式 ,若在标况下消耗11.2L的甲烷,电解NaCl溶液产生的H2的物质的量为 mol(假设燃料电池能量转化率为75%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com