
A.5∶2 B.2∶
解析:为什么等量的纯碱与等量的盐酸反应时,操作不同会有不同体积的CO2产生呢?显然是由于操作不同,反应进程不同所致。操作①:纯碱滴入盐酸中,发生反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O。生成CO2与盐酸用量有关:n(CO2)=1/2n(HCl)=1/2×
Na2CO3+HCl=NaCl+NaHCO3(1)
NaHCO3+HCl=NaCl+CO2↑+H2O(2)
则反应(1)消耗盐酸0.1×1=0.1 mol,生成0.1 mol NaHCO3,过量盐酸(0.025 mol)与NaHCO3反应生成0.025 mol CO2,所以n(CO2)①∶n(CO2)②=0.062 5∶0.025=5∶2。
答案:A


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
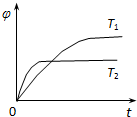 一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:
一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:| A、热化学方程式中:n<p+q | B、热化学方程式中:△H>0 | C、达平衡后,增加A的量,有利于提高B的转化率 | D、若T1、T2时反应的平衡常数分别为K1、K2,则K1>K2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com