
��ҵ�����������ԭ�ϣ�һ���ǻ���������Ҫ�ɷ�ΪFeS2��SΪ-1�ۣ�����һ���ǴŻ���������Ҫ�ɷ���Fe1-xS��SΪ-2�ۣ���ʽ��xͨ��Ϊ0.1~0.2���Ⱥ���Fe2���ֺ���Fe3����
��������ʱ����ʯ���գ�������Ӧ���£�
�� 4 FeS2 + 11 O2 �� 2 Fe2O3 + 8 SO2
�� 4 Fe1-xS + (7-3x) O2 �� 2 (1-x) Fe2O3 + 4 SO2
��1����FeS2 72%�Ļ�����10�֣�����������������98%��Ũ���� �֣���ʯ���������������ʣ���
��2�����Ż�����Fe1-xS��x=0.1����Fe1-xS��Fe2����Fe3�������ʵ���֮��Ϊ ��1��
��3�����տ�ʯʱ��Ϊ�˾����ܵؽ���ʯ�е���ת��ΪSO2����ͨ�����20%�Ŀ���������N2��O2�������Ϊ4��1����������������ɷ֣�������Ż����������պ��ų���������SO2������������ú�x�Ĵ���ʽ��ʾ����
��4����һ�����ĴŻ������������������ᣬ��ַ�Ӧ��������S����2.4g��FeCl2 0.425mol������Һ����Fe3��������Fe1-xS�е�xֵ����ʯ�������ɷֲ������ᷴӦ����
��1��12 ��2�֣�
��2��3.5 ��3�֣�
��3�� ��3�֣�
��3�֣�
��4��0.15 ��4�֣�
��������
���������
��1�����ݹ�ϵʽ�У�FeS2~2H2SO4��
120 196
10t��72% x��98% ���x=12t��
��2���������Ϊxmol��������Ϊymol������x+y=0.9��2x+3y=2�����x=0.7��y=0.2����Ϊ3.5:1��
��3���⣺������4mol SO2������Ҫ1.2 (7-3x)mol��O2����������е�N2Ϊ4.8 (7-3x)mol��
��Ӧ��õ��Ļ���������Ϊ��SO2 4mol��O2 0.2 (7-3x)mol��N2 4.8 (7-3x)mol��
�� SO2���������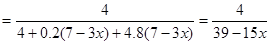
��4���ⷨһ����2Fe3��~S����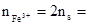 0.15mol
0.15mol
����ԭ���غ�ã�Fe1-xS��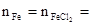 0.425mol��
0.425mol��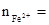 0.275mol
0.275mol
�ɻ��ϼ۵ã� ��0.275
��0.275 2
2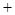 0.15
0.15 3��
3��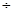 2
2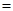 0.5mol
0.5mol
��  ��
�� 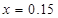
�ⷨ����Fe1-xS + HCl �� FeCl2 + H2S��+ S��
��ԭ���غ�ã�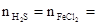 0.425mol ����������Ԫ�ط�Ӧ����H2S�У���Ԫ����FeCl2�У�
0.425mol ����������Ԫ�ط�Ӧ����H2S�У���Ԫ����FeCl2�У�
�� Fe1-xS�� ��Ԫ��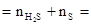 0.075+0.425=0.5mol ��Ԫ��
0.075+0.425=0.5mol ��Ԫ��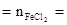 0.425mol
0.425mol
��  ��
�� 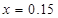
���㣺��ѧ���㣬�غ㷨����ϵʽ����


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��17�֣����ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����衣
��1��ij�¶��£�2SO2��g��+O2��g�� 2S03��g����H3=mkJ/mol��ƽ�ⳣ����K���Ĵ�С���¶ȣ�T���Ĺ�ϵ����ͼ��������ʾ����m____0���>����=����<������b��ʱv������ v���棩���<������=����>��������Ӧ���ʱ䣨��H���� �����������С�����䡱����
2S03��g����H3=mkJ/mol��ƽ�ⳣ����K���Ĵ�С���¶ȣ�T���Ĺ�ϵ����ͼ��������ʾ����m____0���>����=����<������b��ʱv������ v���棩���<������=����>��������Ӧ���ʱ䣨��H���� �����������С�����䡱����
��2������Ӧ����ʼ�����ʵ�����ͬ�����й�ϵͼ����ȷ���� ������ţ���
��3��ij���᳧����SO2β��������м��������ˮ�ϳ��̷���FeS04��7H2O������Ӧ������ԭ���������� ��
��4������Ӧ��Ļ�������ð�ˮ���տɵõ���NH4��2SO3�ͣ�NH4��2SO4���ֻ���ԭ�ϡ�
�ٶ��ڣ�NH4��2SO3��Һ��ijͬѧд�������µ���ȷ��ϵʽ��
2[c��SO2-3��ʮc��HSO-3��+c��H2SO3��]=c��NH+4��+c��NH3��H2O��
�������ͬѧ�������� ��
���ڣ�NH4��2 SO4��Һ�д��ڣ�NH+4+H2O NH3��H2O+H+����÷�Ӧ�����µ�ƽ�ⳣ��K= ����֪�������£�NH3��H2O�ĵ���ƽ�ⳣ��K=1. 7��10-5��
NH3��H2O+H+����÷�Ӧ�����µ�ƽ�ⳣ��K= ����֪�������£�NH3��H2O�ĵ���ƽ�ⳣ��K=1. 7��10-5��
��5�������������պ����õ����᳣�����Ʊ�BaSO4��X������ʱ���ڷ���Ӱ����θ���ǿ��pHԼΪ1���������ô���BaSO4��Ȼ�ǰ�ȫ�ģ�BaSO4���������ԭ���ǣ����ܽ�ƽ��ԭ�����ͣ� ����һ���������BaCO4��Ӧ�����ô���0. 5mol/LNa2SO4��Һ������ϴθ���������ϴθ������Na2SO4��ҺŨ�ȵı仯��������θҺ�е�Ba2+Ũ�Ƚ�Ϊmol/L����֪25��ʱ��Ksp��BaSO4��=1��l0-10 ,Ksp��BaCO3��=1��10-9��.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���Ϻ����ֶ���������4�¸߿�Ԥ�⣨��ģ����ѧ�Ծ��������棩 ���ͣ�������
��ҵ�����������ԭ�ϣ�һ���ǻ���������Ҫ�ɷ�ΪFeS2��SΪ-1�ۣ�����һ���ǴŻ���������Ҫ�ɷ���Fe1-xS��SΪ-2�ۣ���ʽ��xͨ��Ϊ0.1~0.2���Ⱥ���Fe2���ֺ���Fe3����
��������ʱ����ʯ���գ�������Ӧ���£�
�� 4 FeS2 + 11 O2�� 2 Fe2O3 + 8 SO2
�� 4 Fe1-xS + (7-3x) O2�� 2 (1-x) Fe2O3 + 4 SO2
��FeS272%�Ļ�����10�֣�����������������98%��Ũ���� �֣���ʯ���������������ʣ���
���Ż�����Fe1-xS��x=0.1����Fe1-xS��Fe2����Fe3�������ʵ���֮��Ϊ ��1��
���տ�ʯʱ��Ϊ�˾����ܵؽ���ʯ�е���ת��ΪSO2����ͨ�����20%�Ŀ���������N2��O2�������Ϊ4��1����������������ɷ֣�������Ż����������պ��ų���������SO2������������ú�x�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com