
【题目】A、B、C、D、E五种化合物均含有某种常见元素(周期表中前18号),它们的转化关系如图所示,其中A的溶液为澄清的溶液,C为难溶的白色固体,E易溶于水,与A属同类别物质。取A的溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。

(1)写出化学式:A________,B________,C________,D________,E________。
(2)写出下列反应的离子方程式:
A→B:__________________________________________________________;
A→D:___________________________________________________________。
【答案】 KAlO2 Al(OH)3 Al2O3 AlCl3 NaAlO2 AlO2-+2H2O+CO2=Al(OH)3↓+HCO3- AlO2-+4H+===Al3++2H2O
【解析】根据框图,B、C都既能与盐酸反应又能与NaOH溶液反应,应为两性化合物,因B加热分解可生成C,则可知B为Al(OH)3,C为A12O3,则D为AlCl3,E为NaAlO2,取A溶液灼烧,焰色反应为紫色(透过蓝色钴玻璃片),说明A中含有K元素,A能与二氧化碳反应生成Al(OH)3,则A应为KAlO2。
(1)通过以上分析知,A、B、C、D、E分别是KAlO2、Al(OH)3、A12O3、AlCl3、NaAlO2,故答案为:KAlO2;Al(OH)3;A12O3;AlCl3;NaAlO2;
(2)A→B的反应为AlO2-和Al(OH)3的转化,反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;A→D的反应为AlO2-和Al3+的转化,反应的离子方程式为AlO2-+4H+=Al3++2H2O,故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;AlO2-+4H+=Al3++2H2O。


科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
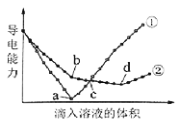
下列分析不正确的是
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH–
C.c点,两溶液中含有相同量的OH–
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→ O2 ,则关于该反应体系说法错误的是
A.该反应的化学方程式为2H2CrO4+3H2O2=2Cr(OH)3+3O2↑+2H2O
B.该反应中的氧化剂是H2O2,还原产物是O2
C.氧化性:H2CrO4>O2
D.如反应转移了0.3mol电子,则产生的气体在标准状况下体积为3.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质燃烧时火焰颜色的描述,不正确的是
A.乙醇在空气中燃烧——淡蓝色B.钠在空气中燃烧——黄色
C.磷在空气中燃烧——绿色D.氢气在氯气中燃烧——苍白色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应: KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:___________________
(2)该反应中还原剂和氧化剂的物质的量之比为______________;
(3)如果反应中转移1mol电子,则生成I2的物质的量为____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 按系统命名法,化合物 的名称为2﹣甲基﹣3,4﹣二乙基己烷
的名称为2﹣甲基﹣3,4﹣二乙基己烷
B. 等物质的量甲烷、乙炔、乙烯分别充分燃烧,所耗用氧气的量依次增加
C. 下列物质的沸点按由低到高顺序为:(CH3)2CHCH3<(CH3)4C<(CH3)2CHCH2CH3<CH3(CH2)3CH3
D. ![]() 与
与![]() 互为同系物
互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分为Al2O3,还有少量杂质)中提取铝的工艺流程及步骤如下:

试回答下列问题:
(1)试剂X为__________;
(2)操作Ⅰ、操作Ⅱ均为_____________(填操作名称),在实验室进行该操作时需要的玻璃仪器有__________________________________;
(3)金属铝与氧化铁混合在高温下,会发生剧烈的反应,该反应的化学方程式为_______________________________,请举一例该反应的用途________________________;
(4)反应Ⅱ的离子方程式为____________________________________________________;
(5)电解熔融氧化铝制取金属铝,若有0.6 mol电子发生转移,理论上能得到金属铝的质量是________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】文学中有“点石成金”,趣味实验中有“点L成M”:取少量白色粉末于烧杯中,加入适量水得蓝色溶液,将金属棒L插入该溶液,一段时间后,在金属棒L表面析出紫红色固体M,溶液颜色变浅。则“点L成M”不可能是
A.点铝成铜B.点银成钠
C.点锌成钙D.点铁成铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com