
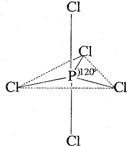
 白磷(P4)是磷的单质之一,易氧化,与卤素单质反应生成卤化磷。卤化磷通常有三卤化磷或五卤化磷,五卤化磷分子结构(以PCl5为例)如右图所示。该结构中氯原子有两种不同位置。
白磷(P4)是磷的单质之一,易氧化,与卤素单质反应生成卤化磷。卤化磷通常有三卤化磷或五卤化磷,五卤化磷分子结构(以PCl5为例)如右图所示。该结构中氯原子有两种不同位置。
1)6.20g白磷在足量氧气中完全燃烧生成氧化物,反应所消耗的氧气在标准状况下的体积为 L。
上述燃烧产物溶于水配成50.0mL磷酸(H3PO4)溶液,该磷酸溶液的物质的量浓度为 mol·L-1。
2)含0.300mol H3PO4的水溶液滴加到含0.500mol Ca(OH)2的悬浮液中,反应恰好完全,生成l种难溶盐和16.2g H2O。该难溶盐的化学式可表示为 。
3)白磷和氯、溴反应,生成混合卤化磷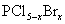 (
( ,且x为整数)。
,且x为整数)。
如果某混合卤化磷共有3种不同结构(分子中溴原子位置不完全相同的结构),该混合卤化磷的相对分子质量为 。
4)磷腈化合物含有3种元素,且分子中原子总数小于20。0.10mol PCl5和0.10mol NH4Cl恰好完全反应,生成氯化氢和0.030mol磷腈化合物。推算磷腈化合物的相对分子质量(提示:M>300)。
【答案】1)5.6;4.00;2)Ca5(PO4)3(OH);3)297.5或342;4)348或464。
【解析】此题考查了元素化合物、化学计算知识。1)白磷燃烧生成五氧化二磷,白磷的相对分子质量为:128,则其6.20g的物质的量为:0.05mol,其完全燃烧消耗氧气0.25mol,标准状况下体积为5.6L;将这些白磷和水反应生成磷酸0.20mol,溶液体积为50mL,也就是0.05L,则磷酸溶液的物质的量浓度为4.00mol/L;2)根据该水溶液中含有溶质的物质的量和氢氧化钙悬浊液中溶质的物质的量,根据质量守恒,可知该物质中含有5个钙离子和3个磷酸根离子,结合电荷守恒,必还含有1个氢氧根离子,写作:Ca5(PO4)3(OH);3)根据题意x为整数,其可能为:PCl4Br、PCl3Br2、PCl2Br3、PClBr4四种,要是有三种不同结构的话,结合PCl5的结构,其可能为:PCl3Br2或PCl2Br3,则其相对分子质量可能为:297.5或342;4)根据题意和质量守恒定律,可求出化合物提供的Cl原子的物质的量为:0.1mol×5+0.1mol×1=0.6mol;由于磷腈化合物中只含有三种元素,故必须将其中的氢原子全部除去;两物质提供的H原子的物质的量为:0.1mol×4=0.4mol,则生成的氯化氢的物质的量为:0.1mol×4=0.4mol;则磷腈化合物中含有的Cl原子为:0.2mol、P原子为:0.1mol、N原子为:0.1mol,则该化合物的最简式为:PNCl2;假设其分子式为(PNCl2)x,由其含有的碳原子总数小于20,则知:4x<20,故x<5;假设x=4,其分子式为: P4N4Cl8,相对分子质量为464;假设x=3,其分子式为: P3N3Cl6,相对分子质量为:348;假设x=2,其分子式为:P2N2Cl4,相对分子质量<300 舍去。故其相对分子质量可能为:348或464。


科目:高中化学 来源: 题型:
新型纳米材料氧缺位铁酸盐(MFe 2Ox3<x<4,M=Mn、Co、Zn或Ni,在该盐中均显+2价)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图。关于此转化过程的叙述不正确的是( )
2Ox3<x<4,M=Mn、Co、Zn或Ni,在该盐中均显+2价)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图。关于此转化过程的叙述不正确的是( )

A.MFe2O4在与H2反应中表现了氧化性
B.MFe2O4与MFe2Ox的相互转化反应均属于氧化还原反应
C.MFe2Ox与SO2反应中MFe2Ox被还原
D.若4 mol MFe2Ox与1 mol SO2恰好完全反应,则MFe2Ox中x的值为3.5
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.Li在氧气中燃烧主要生成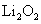
B.将SO2通入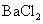 溶液可生成
溶液可生成 沉淀
沉淀
C.将CO2通入次氯酸钙溶液可生成次氯酸
D.将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
有关①100ml 0.1 mol/L 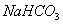 、②100ml 0.1 mol/L
、②100ml 0.1 mol/L 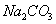 两种溶液的叙述不正确的是
两种溶液的叙述不正确的是
A.溶液中水电离出的 个数:②>① B.溶液中阴离子的物质的量浓度之和:②>①
个数:②>① B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中: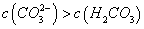 D.②溶液中:
D.②溶液中: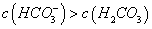
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氯的说法正确的是( )
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.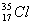 、
、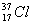 为不同的核素,有不同的化学性质
为不同的核素,有不同的化学性质
C.实验室制备Cl2可用排饱和食盐水集气法收集
D.1.12 L Cl2含有1.7NA个质子(NA表示阿伏加德罗常数)
查看答案和解析>>
科目:高中化学 来源: 题型:
超细氧化铝是一种重要的功能陶瓷原料。
(1)实验室常以NH4Al(SO4)2和NH4HCO3为原料,在一定条件下先反应生成沉淀NH4AlO(OH)HCO3,该沉淀高温分解即得超细Al2O3。NH4AlO(OH)HCO3热分解的化学反应方程式为_________________________。
(2)NH4Al(SO4)2·12H2O的相对分子质量为453。欲配制100 mL pH为2、浓度约为0.1 mol·L-1的NH4Al(SO4)2溶液,配制过程为:
①用托盘天平称量NH4Al(SO4)2·12H2O固体______________________g;
②将上述固体置于烧杯中,_________________________。
(3)在0.1 mol·L-1 NH4Al(SO4)2溶液中,铝各形态的浓度(以Al3+计)的对数(lgc)随溶液pH变化的关系见下图:
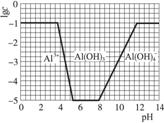
①用NaOH溶液调节(2)中溶液pH至7,该过程中发生反应的离子方程式有___________。
②请在答题卡的框图中,画出0.01 mol·L-1 NH4Al(SO4)2溶液中铝各形态的浓度的对数lgc随溶液pH变化的关系图,并进行必要标注。
查看答案和解析>>
科目:高中化学 来源: 题型:
1995年三位美国科学家因在氟利昂和臭氧层方面的工作获得诺贝尔化学奖,他们的研究揭示了大气中臭氧层被破坏的机理,由图可知( )
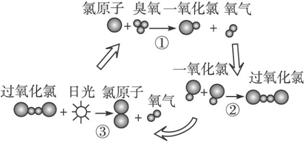
A.日光在反应中作催化剂
B.过氧化氯是一种很稳定的物质
C.过氧化氯的结构式为O—Cl—Cl—O
D.臭氧分子最终转变成氧气分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com