
| A. | 增加反应物的用量一定能增大反应速率 | |
| B. | 化学反应速率只能加快不能减慢 | |
| C. | 决定化学反应速率的主要因素是浓度 | |
| D. | 参加反应物质的性质是决定化学反应速率的主要因素 |
分析 影响化学反应速率的因素有内因和外因,内因为主要因素,是物质的本身性质,而外界因素有浓度、温度、压强以及催化剂等,一般来说增大浓度、升高温度、加入催化剂等,可增大反应速率,以此解答.
解答 解:A.如为固体或纯液体,则增加反应物的用量,浓度不变,故A错误;
B.如降低温度、浓度,可减小反应速率,故B错误;
C.决定化学反应速率的主要因素是物质的本身性质,故C错误;
D.物质的本身性质为影响化学反应速率的主要因素,如钠可与冷水发生剧烈反应,但铜在高温下与水也不反应,故D正确.
故选D.
点评 本题考查化学反应速率知识,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | SO2+2H2S═3S+2H2O | ||
| C. | Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑ | D. | NaOH+HCl═NaCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl中含有共价键,又全部由非金属元素组成,属于共价化合物 | |
| B. | 氮气和氦气都是非金属单质,都不存在化学键 | |
| C. | H2O2和Na2O2 都属于氧化物,两种物质中所含的化学键的类型完全相同 | |
| D. | KOH中既含有离子键也含有共价键,属于离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯和水、酒精和水、苯酚和水 | |
| B. | 二溴乙烷和水、溴苯和水、硝基苯和水 | |
| C. | 甘油和水、乙醛和水、乙酸和乙醇 | |
| D. | 乙酸和水、甲苯和水、己烷和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
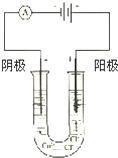 按如图所示装置连接好仪器在U形管中加入饱和氯化铜溶液,用石墨棒作电极,接通电源,电解数分钟后,观察现象.
按如图所示装置连接好仪器在U形管中加入饱和氯化铜溶液,用石墨棒作电极,接通电源,电解数分钟后,观察现象.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
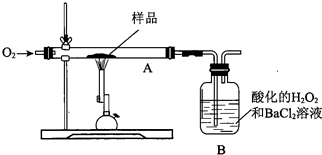
| A. | 测B中沉淀质量 | B. | 测锻烧后A中固体的质量 | ||
| C. | 测B吸收瓶反应前的质量 | D. | 将W蒸干、灼烧,测所得固体质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2g氦气所含原子数为NA | |
| B. | 1molD2O所含电子数为12NA | |
| C. | 0.1mol单质铝与足量盐酸反应转移的电子数为0.3NA | |
| D. | 标准状况下,1L水所含分子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com