
 CH3COOH+OH-的平衡中,要使平衡向右移动,应采取的措施是
CH3COOH+OH-的平衡中,要使平衡向右移动,应采取的措施是| A.加入NaOH固体 | B.加入冰醋酸 | C.增大压强 | D.升高温度 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.25℃时,pH=7的NH4Cl与NH3?H2O混合溶液:c(H+)=c(OH-)=c(NH4+)=c(Cl-) |
| B.0.1mol/LNa2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C.25℃时,pH=2的CH3COOH与pH=12的NaOH等体积混合: c(CH3COO-)+c(H+)<c(Na+)+c(OH-) |
| D.0.1mol/LNa2CO3溶液:2c(CO32-)+2c(HCO-)+2c(H2CO3)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
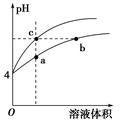
| A.a、c两点溶液的导电能力相同 |
| B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-) |
| C.用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc |
| D.a、b、c三点溶液水的电离程度a>b>c |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(NH4+)相等的(NH4)2SO4和NH4Cl溶液中,溶质浓度大小关系:c[(NH4)2SO4]<c(NH4Cl) |
| B.向10 mL 0.10 mol·L-1的CH3COOH溶液中加入等物质的量的NaOH后,溶液中:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| C.两种不同浓度的HA溶液的物质的量浓度分别为c1和c2,pH分别为a和(a+1),则有c1≥10c2 |
| D.NaHCO3溶液中:c(H+)+c(H2CO3)=c(CO32—)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.10mL 0.2 mol·L-1的氨水与l0mL 0.1 mol·L-1的盐酸充分反应混合后的溶液中,存在c(NH4+)+c(NH3·H2O)=2c(Cl-)= 0.1 mol·L-1 |
| B.已知酸性HF > CH3COOH,物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) - c(F-) >c(K+) - c(CH3COO-) |
| C.CH3COOK溶液中加入少量NaNO3固体后的碱性溶液一定有:c(K+)+c(H+)=c(CH3COO-)+c(OH-) |
| D.已知NaHS03溶液pH<7,该溶液中一定有:c(Na+)> c(HSO3-)> c(SO32-)>c(H2SO3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(Na+)>c(C1-)>c(OH-)>c(H+) |
| B.c(Na+)=c(C1-)>c(OH-)>c(H+) |
| C.c(Na+)=c(C1-)>c(H+)>c(OH-) |
| D.c(C1-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向Na2CO3溶液中滴加酚酞试液变红色 | B.实验室保存硫酸亚铁溶液时加入少量铁粉 |
| C.加热FeCl3溶液颜色会变深 | D.KAl(SO4)2·12 H2O可用于净水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH = 5的NaHSO3溶液:[HSO3-]>[H2SO3]>[SO32-] |
| B.pH = 8的苯酚与苯酚钠混合溶液:[Na+]>[C6H5O-]>[OH-]>[H+] |
| C.pH = 7的CH3COONa与CH3COOH的混合溶液:[Na+]=[CH3COO-]+[CH3COOH] |
| D.0.1 mol/L NaHCO3溶液:[OH-] + [CO32-]= [H+]+[H2CO3] |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 则下列说法正确的是( )
则下列说法正确的是( )| A.Na2CO3溶液中:c(Na+) > c(CO32-) > c(OH-) > c(H+) |
| B.加入NaOH固体,溶液pH减小 |
| C.Na2CO3溶液中:c(Na+) +c(H+) =2c(CO32-) +c(OH-) |
| D.升高温度平衡向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com