
|
下列物质中,前者是电解质,后者是非电解质的是 | |
| [ ] | |
A. |
NaCl、Cl2 |
B. |
NaHCO3、蔗糖 |
C. |
Ba(OH)2、HCl |
D. |
H2SO4、盐酸 |
 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:江苏省南京市白下区2011届高三二模化学试题 题型:022
| |||||||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
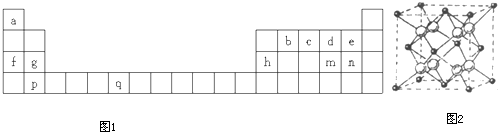
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省苏州五中高三(上)期中化学试卷(解析版) 题型:解答题

查看答案和解析>>
科目:高中化学 来源:江苏模拟题 题型:填空题



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com