
| A. | ls22s22p63s23p5 | B. | 1s22s22p3 | C. | 1s22s22sp5 | D. | 1s22s22p63s23p4 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | 由丙醛与氢气制取丙醇:由丙烯与水反应制丙醇 | |
| B. | 由甲苯硝化制对硝基甲苯:由甲苯氧化制苯甲酸 | |
| C. | 由乙酸和乙醇制乙酸乙酯:由苯甲酸甲酯水解制苯甲酸和甲醇 | |
| D. | 由丙烯与溴水反应制二溴丙烷:由丙烯与氯气加热反应制3-氯丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质能与水反应生成强碱的金属元素都在ⅠA族 | |
| B. | L层上的电子数为奇数的元素一定是主族元素 | |
| C. | 稀有气体元素原子的最外层电子数均为8 | |
| D. | 元素周期表有18个纵行,分列16个族,即7个主族、8个副族和一个零族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CS2为V形的极性分子 | B. | ClO3-的空间构型为平面三角形 | ||
| C. | SF6中有6对完全相同的成键电子对 | D. | SiF4和SO3的中心原子均为sp2杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子的最外层电子数比B原子最外层电子数少 | |
| B. | 常温下,A能从冷水中置换出氢气,而B不能 | |
| C. | 等物质的量A和B与足量稀硫酸反应,产生氢气的量A比B多 | |
| D. | A原子的电子层数比B原子电子层数多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加某一反应物的用量一定能够加快该反应的速率 | |
| B. | 化学反应的限度是不可改变的 | |
| C. | 化学反应进行的时间越长该反应的限度越大 | |
| D. | 化学反应达到限度时,正逆反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
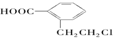 ,A在一定条件下有如图所示的转化关系.已知E分子式为C9H8O2.
,A在一定条件下有如图所示的转化关系.已知E分子式为C9H8O2.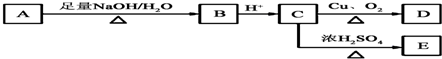
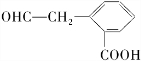 ,若E能使溴的四氯化碳溶液褪色,还能与NaHCO3溶液反应生成F,欲由A通过一步反应得到F,该反应的化学方程式是
,若E能使溴的四氯化碳溶液褪色,还能与NaHCO3溶液反应生成F,欲由A通过一步反应得到F,该反应的化学方程式是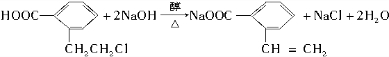 .
. ,写出所有符合下列要求的E的同分异构体的结构简式:
,写出所有符合下列要求的E的同分异构体的结构简式: 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a-n-3 | B. | a+n+3 | C. | a+n-3 | D. | a-n+3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com