
����Ŀ����ѡ��-ѡ��5: �л���ѧ������PET��PMMA���ճ�����������ָ߷��Ӳ��ϡ������Ǻϳɸ߷��Ӳ��ϵ�·��:

��֪:��RCOOR1+R2OH![]() RCOOR2+R1OH
RCOOR2+R1OH
�� (R1��R2��ʾ��������ԭ��)
(R1��R2��ʾ��������ԭ��)
�ش���������:
(1)����A�Ļ�ѧ����_______������H�й����ŵ�����________��
(2)��C����D��I����J�ķ�Ӧ���ͷֱ���_______��_______��
(3)��I����J�ķ�Ӧ�в�����Ԫ���ĸ������ṹ��ʽΪ_______��
(4)д��D+�Ҷ�����F+G�Ļ�ѧ��Ӧ����ʽ________________��
(5)D���ڶ���ͬ���칹�壬����ֻ����һ�ֹ����ŵ���ȡ�������廯����������̼��������Һ���ò��������ͬ���칹����____�֡�
(6)д���û�����Ϊԭ���Ʊ� �ĺϳ�·��(�����Լ���ѡ)_________��
�ĺϳ�·��(�����Լ���ѡ)_________��
���𰸡� �Զ��ױ�����1��4-���ױ��� ȩ�� ������ȡ������Ӧ ��ȥ��Ӧ 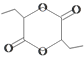
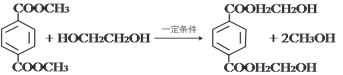 16
16 ![]()
��������(1)��A�ķ���ʽΪC8H10,���ϱ���ͬϵ���ͨʽ������AΪ����ͬϵ���D���Ʒ�֪A��������Ӧ���ڱ����Ķ�λ����A�Ľṹ��ʽΪ ����������A�Ļ�ѧ���ƶԶ��ױ�����1��4-���ױ���������Ϣ��
����������A�Ļ�ѧ���ƶԶ��ױ�����1��4-���ױ���������Ϣ��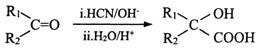 ��
��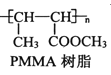 ����֪KΪ
����֪KΪ![]() �����G����J�Ľṹ��ʽΪCH3CH=C(OH)COOH,I�Ľṹ��ʽΪCH3CH2C(OH)COOH,��֪����H�Ľṹ��ʽΪCH3CH2CHO,H�й����ŵ�����ȩ����
�����G����J�Ľṹ��ʽΪCH3CH=C(OH)COOH,I�Ľṹ��ʽΪCH3CH2C(OH)COOH,��֪����H�Ľṹ��ʽΪCH3CH2CHO,H�й����ŵ�����ȩ����
���ݷ�Ӧ������A�Ľṹ��ʽ ![]() ��
��![]() ֪B�Ľṹ��ʽΪ
֪B�Ľṹ��ʽΪ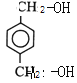 ����
����![]() ֪C�Ľṹ��ʽΪ��
֪C�Ľṹ��ʽΪ��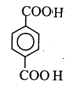 ��
�� 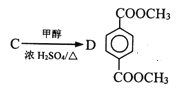 ��������D�ķ�Ӧ������������ȡ������Ӧ��
��������D�ķ�Ӧ������������ȡ������Ӧ��
�� ����֪KΪ
����֪KΪ![]() �����G����J�Ľṹ��ʽΪCH3CH=C(OH)COOH,I�Ľṹ��ʽΪCH3CH2C(OH)COOH, ����I����J�ķ�Ӧ����Ϊ��ȥ��Ӧ���𰸣�������ȡ������Ӧ ��ȥ��Ӧ��
�����G����J�Ľṹ��ʽΪCH3CH=C(OH)COOH,I�Ľṹ��ʽΪCH3CH2C(OH)COOH, ����I����J�ķ�Ӧ����Ϊ��ȥ��Ӧ���𰸣�������ȡ������Ӧ ��ȥ��Ӧ��
(3)������������I�Ľṹ��ʽΪCH3CH2C(OH)COOH����J�ķ�Ӧ�в�����Ԫ�������ʵ���ṹ��ʽΪ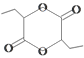
(4)��D�Ľṹ��ʽΪ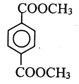 ���Ҷ����ķ�Ӧ��Ӧ����ʽΪ
���Ҷ����ķ�Ӧ��Ӧ����ʽΪ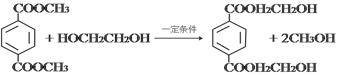
(5)D���ڶ���ͬ���칹�壬����ֻ����һ�ֹ����ŵ���ȡ�������廯����������̼��������Һ���ò��������ͬ���칹����16�֡�
 ��10�֣�
��10�֣�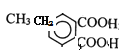 (6��)
(6��)
(6)�û�����Ϊԭ���Ʊ�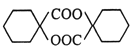 �ĺϳ�·��Ϊ
�ĺϳ�·��Ϊ![]()



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���з�Ӧ���Ȼ�ѧ����ʽ��
��6C��s��+5H2��g��+3N2��g��+9O2��g��=2C3H5(ONO2)3��l����H1
��H2��g��+![]() O2��g��=H2O��g����H2
O2��g��=H2O��g����H2
��C��s��+O2��g��=CO2��g����H3
��4C3H5(ONO2)3��l��=12CO2��g��+10H2O��g��+O2��g��+6N2��g����H4
����˵������ȷ���ǣ� ��
A. ��H4=12��H3+10��H2��2��H1
B. �������� H2��g����Ϊ H2��l�����H����H1
C. C�����ʯ��s���� C��ʯī��s����ȼ���Ȳ�ͬ
D. ��H2�� H2��g����ȼ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ǷŴ��˵ط�����Դ����Ӧ����������á������з��������ϴ�����ֽ��������Ʒ������
A. ���� B. ��� C. ���� D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����ࡢ��Ч����Դ��Ҳ����Ҫ�Ļ���ԭ�ϡ�
(1)��ҵ�����ü����Ʊ������ķ�ӦΪ:CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
��֪:
��H2(g)+![]() O2(g)=H2O(g) ��H1=-198kJ/mol
O2(g)=H2O(g) ��H1=-198kJ/mol
��2CO(g)+O2(g)=2CO2(g) ��H2=-576kJ/mol
��CH4(g)+2O2(g)=CO2(g)+2H2O(g) ��H3=-846.3kJ/mol
��CH4(g)+H2O(g)![]() CO(g)+3H2(g) ��H4=________��
CO(g)+3H2(g) ��H4=________��
(2)��ҵ������CO��H2�ϳ������ԴCH3OH,�䷴ӦΪ:CO(g)+2H2(g)![]() CH3OH(g) ��H=-116kJ/mo1
CH3OH(g) ��H=-116kJ/mo1
����ͼ��ʾCO��ƽ��ת����(��)���¶Ⱥ�ѹǿ�仯��ʾ��ͼ��X��ʾ����_______������_________��Y1_____Y2 (�<������=������>��)��
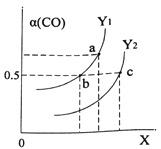
����2L�����ܱ������г���2molCO��4molH2����һ�������¾���10min�ﵽƽ��״̬c �㴦�����ڸ������£��ӿ�ʼ���ﵽƽ��״̬v(CH3OH)=________��ƽ�ⳣ��Ka��Kb��Kc�Ĵ�С��ϵ:____________��
�����д�ʩ��������Ӧ����������߷�Ӧ���ת���ʵ���_______��
A.ʹ�ô��� B.��ʱ����CH3OH C.�����¶� D.����ѹǿ
(3)��֪ȼ�ϵ�صı������뵥λ����ȼ������ʧȥ�ĵ����������ȡ�������H2��CH4��CH3OH�ļ��Ե�صı�������С�����˳��Ϊ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѡ��-ѡ��3:���ʽṹ�����ʡ�����п��һ�ְ뵼����ϣ��ش��������⡣
(1)п�����ڱ��е�λ��_______��Se��̬ԭ�Ӽ۵����Ų�ͼΪ______��Ԫ��п���������һ�����ܽϴ����________(��Ԫ�ط���)��
(2)Na2SeO3������Seԭ�ӵ��ӻ�����Ϊ_______��H2SeO4�����Ա�H2SeO3ǿ��ԭ����_______��
(3)��̬SeO3���ӵ����幹��Ϊ_______��������SeO3��Ϊ�ȵ��������__(�����)��
A.CO32- B.NO3- C.NCl3 D.SO32-
(4)����п�ľ����ṹ��ͼ��ʾ��ͼ��X��Y�����ѻ���ԭ�Ӿ�Ϊ______(��Ԫ�ط���)���þ�������ԭ��������϶����Ϊ_____(������塱�����������塱���������塱)������Ʒ�����ܶ�Ϊ��g/cm3������п��Ħ������ΪMg/mol����NA���������ӵ���������ֵ��������aΪ_______nm��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����
A. ����ʯ��ˮ�����̼��������Һ��Ӧ��![]() +Ca2++OH��=CaCO3��+H2O
+Ca2++OH��=CaCO3��+H2O
B. ����������Һ�м�������������Һ�����ԣ�H++![]() +Ba2++OH��=BaSO4��+2H2O
+Ba2++OH��=BaSO4��+2H2O
C. ������������Һ��ͨ������CO2��2OH��+CO2=![]() +H2O
+H2O
D. ������������Һ�м���������2H++![]() +Ba2++2OH��=BaSO4��+2H2O
+Ba2++2OH��=BaSO4��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ά�ر���Ϊ����Ӫ���أ�ʳ���е���ά����Ȼ����Ϊ�����ṩ���������ܴٽ������䶯�������ų��к����ʣ�����ά�صĻ�ѧ�ɷֿ�������һ��
A. ���� B. ���� C. ������ D. ֬��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���ԷϾɵĺ�������(��Ҫ�ɷ�ΪNiO������Fe2O3��CaO��CuO��BaO��)Ϊԭ����ȡNi2O3��������������ͼ��
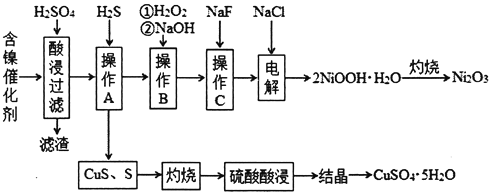
��������������������pH��������ʵ��ܽ������±���
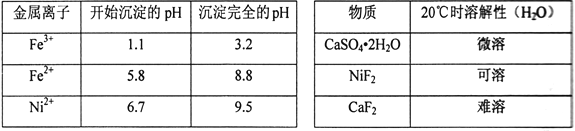
�ش��������⣺
��1����������Ҫ�ɷ�ΪBaSO4��____________________(�ѧʽ)��
��2������A�з�����Ӧ�����ӷ���ʽΪCu2++H2S=CuS��+2H+��_________________________������A��û��FeS��NiS������������ԭ����(��Ka��Ksp����)__________________________��
��3������B����H2O2��Ŀ����________________����NaOH��Һ����pHӦ��____________��Χ�ڣ�����C�м���NaF��Ŀ����____________________��
��4���ù���������ʹ��H2S���壬�ŵ��ǿ�����ȡ����ƷCuSO4��5H2O����Ҳ�����Ե�ȱ�㣺һ�Dz���������Ⱦ������______________________________________________��
��5��������2NiOOH��H2O��ԭ��Ϊ���ڼ��������µ�⣬Cl-������������ΪClO-��ClO-�ٽ�Ni2+������2NiOOH��H2O�������������ĵ缫��ӦʽΪ________________________��
��6��0.80g CuSO4��5H2O����Ʒ������ˮ���̵���������(��Ʒ�������¶ȱ仯������)��ͼ��ʾ��CuSO4��5H2O�ȶ����ڵ��¶�Ӧ����________����200��ʱ�������ʵĻ�ѧʽ____________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�����ڱ��У�Ԫ��A��Bλ��ͬ���ڣ�A�ڢ�A�壬B�ڢ�A�塣A��ԭ������Ϊa��B��ԭ������Ϊb����������(����)
A.b��a+1B.b��a+11
C.b��a+10D.b��a+25
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com