
| A. | ${\;}_{6}^{12}$C、${\;}_{6}^{13}$C、${\;}_{6}^{14}$C是碳元素的三种核素 | |
| B. | SO2分子中含有离子键 | |
| C. | MgCl2固体中含有共价键 | |
| D. | ${\;}_{8}^{16}$O、${\;}_{8}^{17}$O、${\;}_{8}^{18}$O含有相同的中子数 |
分析 A.质子数相同、中子数不同的同一元素不同元素互称同位素,同位素属于不同的核素;
B.非金属元素之间易形成共价键;
C.活泼金属和活泼非金属元素之间易形成离子键;
D.中子数=质量数-质子数.
解答 解:A.质子数相同、中子数不同的同一元素不同元素互称同位素,同位素属于不同的核素,${\;}_{6}^{12}$C、${\;}_{6}^{13}$C、${\;}_{6}^{14}$C的质子数相同、中子数不同,是碳元素的三种核素,故A正确;
B.非金属元素之间易形成共价键,二氧化硫中只含共价键,故B错误;
C.活泼金属和活泼非金属元素之间易形成离子键,氯化镁中只含离子键,故C错误;
D.中子数=质量数-质子数,${\;}_{8}^{16}$O、${\;}_{8}^{17}$O、${\;}_{8}^{18}$O的中子数分别是8、9、10,所以中子数不同,故D错误;
故选A.
点评 本题考查化学键、核素等知识,侧重考查基本概念,明确离子键和共价键的区别是解本题关键,知道质子数、中子数和质量数的体系,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
| 编 号 | 猜 想 |
| 甲 | 溶液中的+3价Fe又被还原为+2价Fe |
| 乙 | 溶液中的+3价Fe被氧化为更高的价态 |
| 丙 | 新制的氯水具有漂白性,将该溶液漂白 |
| 丁 | ? |
| 实验操作 | 预期现象 | 结 论 |
| 说明丁同学的猜想是合理的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H5CH2Cl+NaCN-→C6H5CH2CN+NaCl | B. | 2Na+2 C2H5OH-→2C2H5ONa+H2↑ | ||
| C. | CH3CH2CHO+HCN-→CH3CH2CH(CN)OH | D. | CH3COOC2H5+H2O-→CH3COOH+C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小 | |
| C. | 放热反应在常温下一定很容易发生 | |
| D. | 化学反应一定有新物质的生成,但不一定有能量的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第二周期元素从左到右,最高正价从+1递增到+7 | |
| B. | ⅠA和ⅦA族元素间可形成离子化合物和共价化合物 | |
| C. | 同主族元素的简单阴离子还原性越强,元素非金属性越强 | |
| D. | 同周期金属元素的化合价越高,其金属性越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
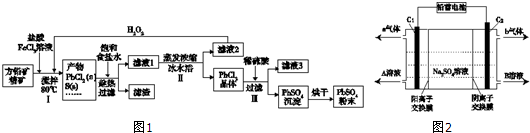
| Ksp | 开始沉淀时pH | 完全沉淀时pH | ||
| PbSO4 | 1.08×10-8 | Fe (OH)3 | 2.7 | 3.7 |
| PbCl2 | 1.6×10-5 | Pb( OH)2 | 6 | 7.04 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其水溶液显弱酸性,俗称石炭酸 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 苯酚溶液不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 依据原子序数,推断该元素原子的核外电子数 | |
| B. | 依据相对分子质量,推断物质常温下的溶解度 | |
| C. | 依据气体的摩尔质量,推断相同状况下不同气体密度的大小 | |
| D. | 依据元素原子的最外层电子数,推测其可能的最高正价和最低化合价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com