
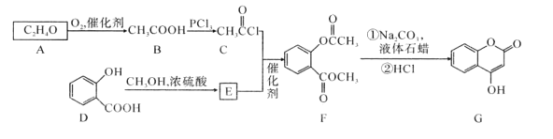
����Ŀ���л�������G��4-�ǻ��㶹�أ�����Ҫ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɡ�
��ش�
��1��D��E�ķ�Ӧ������___��
��2��G�к��еĹ���������Ϊ____��
��3��д��G����NaOH��Һ����ʱ��Ӧ�Ļ�ѧ����ʽ___��
��4��������E��ͬ���칹��ܶ࣬�������������Ľṹ��___�֡�
�������Ȼ�����Һ������ɫ��Ӧ�����ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ
���У��˴Ź�������Ϊ5��壬�ҷ������Ϊ2��2��2��1��1�Ľṹ��ʽΪ____��
��5��E��ͬ���칹��ܶ࣬����ͬ���칹��������ij�ֱ�����������ʾ���ź�(������)��ȫ��ͬ����������___(����)��
a.������ b.Ԫ�ط����� c.��������� d.�˴Ź�����
��6����֪���ǻ�һ�㲻��ֱ�������������������ᱽ����(![]() )��һ����Ҫ���л��ϳ��м��塣���������֪ʶ����������Ϣ����д���Ա��ӡ��ױ�Ϊԭ����ȡ�û�����ĺϳ�·������ͼ(��ԭ����ѡ)��___��
)��һ����Ҫ���л��ϳ��м��塣���������֪ʶ����������Ϣ����д���Ա��ӡ��ױ�Ϊԭ����ȡ�û�����ĺϳ�·������ͼ(��ԭ����ѡ)��___��
���𰸡�������Ӧ��ȡ����Ӧ�� ̼̼˫�����ǻ�������  13
13 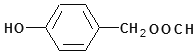 B
B 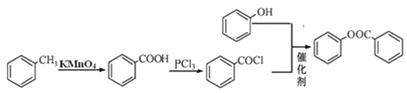
��������
A������������B�����A����ʽ֪AΪCH3CHO��B����ȡ����Ӧ����C��D����������Ӧ����EΪ![]() ��CE����ȡ����Ӧ����F��F������Ӧ����G��
��CE����ȡ����Ӧ����F��F������Ӧ����G��
��1��D��EΪ������Ӧ��ȡ����Ӧ����
��2��GΪ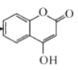 ������������Ϊ̼̼˫�����ǻ���������
������������Ϊ̼̼˫�����ǻ���������
��3��G�к��������ᷢ��ˮ�⣬ˮ��֮�������Ȼ��ͷ��ǻ����������Ʒ�����Ӧ������ʽΪ�� ��
��
��4��EΪ![]() ����ͬ���칹�������������������Ȼ�����Һ������ɫ��Ӧ˵����Ӧ���ǻ������ܷ���������Ӧ˵������-CHO�ṹ�����ܷ���ˮ�ⷴӦ˵������������
����ͬ���칹�������������������Ȼ�����Һ������ɫ��Ӧ˵����Ӧ���ǻ������ܷ���������Ӧ˵������-CHO�ṹ�����ܷ���ˮ�ⷴӦ˵������������
���ȡ����ΪHCOO-��-OH��-CH3����10�֣�
���ȡ����ΪHCOOCH2-��-OH�����ڼ��3�֣�
�������������13�֣�
���У��˴Ź�������Ϊ5��壬�ҷ������Ϊ2��2��2��1��1�Ľṹ��ʽΪ ��
��
��5��A. �����Ƿ���ͼ�ⲻͬͬλ�ص���������A��ѡ��
B. Ԫ�ط�������Ϊһ��ʵ���ҳ�����������ͬʱ���л��Ĺ��塢�ӷ��Ժ�������������C��H��O��N��Cl��Br��Ԫ�صĺ������ж��������ⶨ��ͬ���칹������Ԫ�����������ͬ����Bѡ��
C. ������������������ʶԲ�ͬ�����ĺ��������������ԣ����з��ӽṹ�ͻ�ѧ��ɷ�����������ͬ���칹��֮��ṹ��ͬ����C��ѡ��
D. �˴Ź����ǿ��Բⶨԭ�Ӻ˵��������H�˴Ź����Բⶨ�л�����Hԭ�ӵ��������D��ѡ��
����������ѡB��
��6���Ա��ӡ��ױ�Ϊԭ����ȡ![]() ��
��![]() ���ɱ��Ӻͱ������ȷ���ȡ����Ӧ�õ����������ȿ��ɱ����ᷢ��ȡ����Ӧ�õ����ױ������Ը��������Һ�������ɱ����ᣬ��ϳ�·��Ϊ
���ɱ��Ӻͱ������ȷ���ȡ����Ӧ�õ����������ȿ��ɱ����ᷢ��ȡ����Ӧ�õ����ױ������Ը��������Һ�������ɱ����ᣬ��ϳ�·��Ϊ ��
��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ѧϰ��ѧ����Ҫ���ߡ�����������ʾ���ʱ仯�Ļ�ѧ������������( )
A.ϡ������Һ��ϡ�������Ƶ��к��ȣ�H��(aq)��OH��(aq)��H2O(l) ��H����57.3 kJ�� mol��1
B.FeCl3��Һˮ������ӷ���ʽ��Fe3��+3H2O![]() Fe (OH)3+3H+
Fe (OH)3+3H+
C.�Ȼ�ѧ����ʽΪ��N2(g)+3H2(g)![]() 2NH3(g) ��H=-38.6kJ��mol��1��һ�������£���0.5mol N2(g)��1.5molH2(g)�����ܱյ������з�Ӧ����NH3(g)�������19.3kJ
2NH3(g) ��H=-38.6kJ��mol��1��һ�������£���0.5mol N2(g)��1.5molH2(g)�����ܱյ������з�Ӧ����NH3(g)�������19.3kJ
D.CO(g)��ȼ������283.0 kJ��mol��1����2CO2(g)��2CO(g)+O2(g) ��H=+566.0 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2�ͼ�����ϳ�CO��H2��CO2��Դ�����õ���Ч;������Ҫ��ӦΪ
����CH4��g��+CO2��g��![]() 2CO��g��+2H2��g�� ��H=+247kJ/mol
2CO��g��+2H2��g�� ��H=+247kJ/mol
��1����֪CH4��g��+H2O��g��![]() CO��g��+H2��g�� ��H=+206kJ/mol
CO��g��+H2��g�� ��H=+206kJ/mol
д��CH4��ˮ������Ӧ����CO2���Ȼ�ѧ����ʽ_______________________________��
��2���ں��¡����ݵ��ܱ������з�����ӦI������ѡ���ܹ�˵����ӦI�ﵽƽ��״̬����______��
A.���������ܶȲ���
B.����������ѹǿ����
C.CH4��CO2��CO��H2�����ʵ���֮��Ϊ1:1:2:2
D.3v����H2��=v����CH4��
E.��������ƽ����Է�����������
��3����CH4��CO2��1mol����ij�ܱ������У�������ӦI��100kPaʱ����ӦI����ƽ��ʱCO2������������¶ȵĹ�ϵ������ͼ��ʾ��

��ͼ��A��B��C�����ʾ��ͬ�¶ȡ�ѹǿ�´ﵽƽ��ʱCO2�������������______���Ӧ��ƽ�ⳣ����С���ж�������______________________________��________���Ӧ��ѹǿ���
��300����100kPa�£��������з�ӦI����40min�ﵽƽ�⣬���㷴Ӧ��0-40min�ڵ�ƽ����Ӧ����Ϊv��CO2��=_________mol/min�����������λ��Ч���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʴ�йص�˵����ȷ���ǣ�������
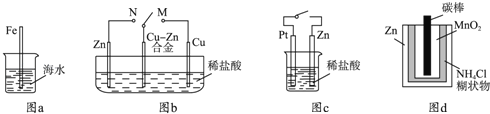
A.ͼa�У����뺣ˮ�е�������Խ�����˸�ʴԽ����
B.ͼb�У�������M������Nʱ��Cu��Zn�Ͻ�ĸ�ʴ���ʼ�С
C.ͼc�У���ͨ����ʱZn��ʴ��������Zn�Ϸų����������Ҳ����
D.ͼd�У�Zn��MnO2�ɵ���Էŵ縯ʴ��Ҫ����MnO2���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Ԫ����H2A��Һ������ʽ�������룺H2A![]() H����HA����HA��
H����HA����HA��![]() H����A2��������������Һ��c(A2��)������(����)
H����A2��������������Һ��c(A2��)������(����)
A.0.01 mol��L��1��H2A��Һ
B.0.01 mol��L��1��NaHA��Һ
C.0.02 mol��L��1��������0.04 mol��L��1��NaHA��Һ��������Һ
D.0.02 mol��L��1��NaOH��0.02 mol��L��1��NaHA��Һ��������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ��CuS��MnS��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵��������ǣ� ��

A.���¶��£�Ksp(CuS)С��Ksp(MnS)
B.��CuSO4��Һ�м���MnS�������·�Ӧ��Cu2��(aq)��MnS(s)=CuS(s)��Mn2��(aq)
C.�ں���CuS��MnS�������Һ��c(Cu2��)��c(Mn2��)Ϊ2��10��23��1
D.a���Ӧ��Ksp����b���Ӧ��Ksp
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�����о�������Ʒ�ĸ�ʴ��װ�õ����������ã��ҿ�ʼʱU�ι����˵ĺ�īˮҺ����ƽ��һ��ʱ����ܹ۲쵽�������⡣����˵������ȷ���ǣ� ��
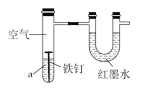
A. �������淢���ķ�ӦΪFe��3e-=Fe3+
B. ��Һ��aΪϡ���ᣬ��U�ι�Һ���Ҹ����
C. ��Һ��aΪʳ��ˮ����U�ι�Һ������ҵ�
D. ��Һ��aΪʳ���ͣ��������������ʽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Ƭ��Ҫ�ɷ�ΪKMnO4������������ɱ������ij���̿�(��Ҫ�ɷ���MnO2��������A12O3��SiO2������)�Ʊ�KMnO4������ͼ���£�

��֪��K2MnO4�������Һ��Ϊī��ɫ����Һ�ʼ������ܷ���������绯��Ӧ��
(1)������I���в�������������____________������������ʱ����__________ʱ��ֹͣ���ȣ���Ȼ��ȴ�����˺ɻ���Ϻ�ɫKMnO4���塣
(2)������ȡҺ����ͨ��CO2��������pH������������������I������I�ijɷ�Ϊ__________��
(3)������������ʱ��MnO2���뷴Ӧ�Ļ�ѧ����ʽΪ_________________________��
(4)���绯��ʱ������������Ŀ����___________________________(�ñ�Ҫ�����ӷ���ʽ�����ֽ���)��
(5)���绯��ʱ���������������������������___________(����ĸ)��
a��Ũ���� b�������� c��ϡ���� d�������
(6)��ȡ�����У���pH���ڲ�����������Mn2+���ڷ�ˮ���������г���H2S��Mn2+ת��ΪMnS��ȥ����0.05mol��L-1Mn2+��ˮ��ͨ��һ����H2S���壬������Һ��pH=a����HS-Ũ��Ϊ1.0��10-4mol��L-1ʱ��Mn2+��ʼ��������a=__________��[��֪��H2S��Ka1=1.3��10-7 Ka2=5.0��10-15��Ksp(MnS)=2.5��10-14]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���J���ڴ�λ����ϵ���е�һ������,���л������������ʮ����Ҫ�ļ�ֵ.2018���ҹ��״�ʹ����������ʻ�������ϳɴ�λ����J,��ϳ�·������:

��֪��
�ش���������:
(1)A ������___________________.
(2)C ��D�Ļ�ѧ����ʽ_________________________.E ��F�ķ�Ӧ����____
(3)H �к��еĹ�����________________.J�ķ���ʽ_______________.
(4)������X��D��ͬ���칹��,������������������Һ��Ӧ��X��_____________��(�����������칹),д�����к˴Ź���������3���,�����֮��Ϊ1��1��6�Ľṹ��ʽΪ___________________________.
(5)�������кϳ�·��ͼ���漰�Լױ��� Ϊԭ�����ϳ���һ�ִ�λ����
Ϊԭ�����ϳ���һ�ִ�λ���� �ĺϳ�·�ߣ�__________________��
�ĺϳ�·�ߣ�__________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com