
分析 A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应,则A为Na元素;5.8g B的氢氧化物恰好能与100mL 2mol•L-1盐酸完全反应,则n(H+)=n(OH-),设B的化合价为x,摩尔质量为y,则$\frac{5.8}{17x+y}$×x=0.2,显然x=2,y=24符合,B原子核中质子数和中子数相等,则B的质子数为12,即B为Mg元素;H2在C单质中燃烧产生苍白色火焰,则C为Cl元素;D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,即D为O元素.
解答 解:A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应,则A为Na元素;5.8g B的氢氧化物恰好能与100mL 2mol•L-1盐酸完全反应,则n(H+)=n(OH-),设B的化合价为x,摩尔质量为y,则$\frac{5.8}{17x+y}$×x=0.2,显然x=2,y=24符合,B原子核中质子数和中子数相等,则B的质子数为12,即B为Mg元素;H2在C单质中燃烧产生苍白色火焰,则C为Cl元素;D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,即D为O元素,
(1)元素C为Cl元素,位于第三周期第ⅦA族,最高价氧化物的化学式为:Cl2O7,
故答案为:三;ⅦA;Cl2O7;
(2)A与D形成稳定的化合物的化学式为Na2O2,属于离子晶体,与CO2反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:Na2O2;离子晶体;2Na2O2+2CO2=2Na2CO3+O2;
(3)C元素的单质氯气有毒,A的最高价氧化物对应的水化物为NaOH,用氢氧化钠溶液吸收氯气的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
点评 本题考查位置结构性质的关系及应用,利用讨论法确定B元素是解答本题的关键,熟悉掌握元素及其单质、化合物的性质,难度中等.


 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
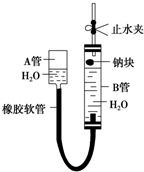 如图是某化学学习小组用来探究钠与水反应的实验装置.该装置可以集反应、收集、检验气体于一体.图中钠块是用大头针叉住的.请填空:
如图是某化学学习小组用来探究钠与水反应的实验装置.该装置可以集反应、收集、检验气体于一体.图中钠块是用大头针叉住的.请填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中三个碳原子可能处于同一直线上 | |
| B. | 全氟丙烷的电子式为: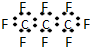 | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 全氟丙烷分子中既有极性键又有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
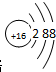 .
.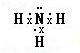 .
.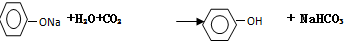 .
.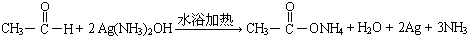 .
.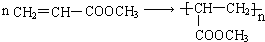 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L CCl4中含有氯原子数目为4 NA | |
| B. | 7 g C2H4中含有的氢原子数目为NA | |
| C. | 1 mol Al 失去电子变成 Al3+后质子数目为10 NA | |
| D. | 1 L 0.5 mol/L Na2CO3溶液中含有的CO32-数目为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅硬度大、熔点高,因而可用于制作半导体材料 | |
| B. | 常温下铝制品可以储运浓硫酸和浓硝酸 | |
| C. | 水煤气、液氯、水玻璃、福尔马林为混合物 | |
| D. | 金属汞一旦洒落在实验室地面或桌面上,必须尽快收集,并深埋处理 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com