
同温同压下,两个容积相等的储气瓶,一个装有C2H4,另一个装有C2H2`
和C2H6的混合气体,两瓶内的气体一定具有相同的( )
A.质量 B.原子总数
C.碳原子数 D.密度
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-1练习卷(解析版) 题型:选择题
下列叙述中正确的是( )
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成
B.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2
C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D.向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-1练习卷(解析版) 题型:选择题
下列各项中所列举的物质与所属类别对应不正确的是( )
A.化合物:干冰,冰水混合物,烧碱,小苏打
B.非电解质:乙醇,四氯化碳,氯气,葡萄糖
C.同素异形体:活性炭,C60,石墨烯,金刚石
D.混合物:铝热剂,纯净矿泉水,盐酸,漂白粉
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-3练习卷(解析版) 题型:选择题
下列所得溶液的物质的量浓度等于0.1 mol·L-1的是( )
A.将0.1 mol氨充分溶解在1 L水中
B.将10 g质量分数为98%的硫酸与990 g水混合
C.将8 g三氧化硫溶于水并配成1 L溶液
D.将0.1 mol氧化钠溶于水并配成1 L溶液
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-2练习卷(解析版) 题型:选择题
用酸性氢氧燃料电池电解饱和食盐水的装置如图所示(a、b为石墨电极,不考虑U形管
中气体的溶解且a上产生的气体全部进入小试管中)。下列说法中错误的是( )
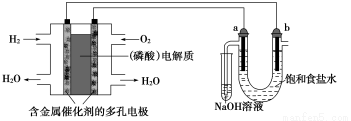
A.同温同压下,燃料电池中参与反应的H2和O2的体积之比为2∶1
B.同等条件下,U形管a、b两端产生的气体的密度之比为35.5∶1
C.燃料电池中消耗0.2 g H2时,U形管中阴极产生的气体为2.24 L(标准状况下)
D.燃料电池中消耗1 mol O2时,小试管中反应转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-1练习卷(解析版) 题型:实验题
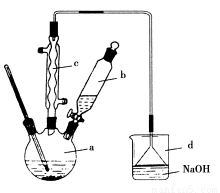
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
| 苯 | 溴 | 溴苯 |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了________气体。继续滴加至液溴滴完。装置d的作用是____________;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是______________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必须的是________(填入正确选项前的字母);
A.重结晶 B.过滤C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是________(填入正确选项前的字母)。
A.25 mL B.50 mLC.250 mL D.500 mL
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-1练习卷(解析版) 题型:选择题
根据以下叙述制备氯化铜:先将浓盐酸用蒸汽加热至80 ℃左右,慢慢加入含有FeO杂质的CuO粉,充分反应,使其溶解。已知:FeS不溶于水,但溶于酸。
溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥9.6 | ≥6.4 |
在除去溶液中的Fe2+时,可采用的方法是( )
A.可直接加碱,调整溶液的pH≥9.6
B.加入纯铜粉,将Fe2+还原为Fe
C.先将Fe2+氧化成Fe3+,再调整溶液pH至3~4
D.通入H2S使Fe2+直接沉淀
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习2-3-2氧化还原反应方程式配平及计算练习卷(解析版) 题型:选择题
24 mL浓度为0.05 mol·L-1的Na2SO3溶液恰好与20 mL浓度为0.02 mol·L-1的K2Cr2O7溶液完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为 ( )。
A.+2 B.+3 C.+4 D.+5
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十二 仪器组合型专题练习卷(解析版) 题型:选择题
用下列装置不能达到有关实验目的的是( )
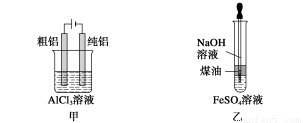

A.用甲图装置电解精炼铝
B.用乙图装置制备Fe(OH)2
C.丙图装置酸性KMnO4溶液中出现气泡且颜色逐渐褪去
D.用丁图装置验证NaHCO3和Na2CO3的热稳定性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com