
�ڻ�ѧ��Ӧ�У�ֻ������������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ���ܷ�����ѧ��Ӧ�����ǰ���������ѧ��Ӧ����ײ��Ϊ��Ч��ײ��������Ч��ײ�ķ��ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λ��kJ•mol-1��ʾ������۲���ͼ��Ȼ��ش����⡣
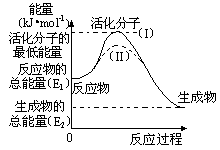 ��1��ͼ�з�Ӧ�� ������ȡ����ȡ�����Ӧ���÷�Ӧ�ġ�H= ���ú�E1��E2�Ĵ���ʽ��ʾ����
��1��ͼ�з�Ӧ�� ������ȡ����ȡ�����Ӧ���÷�Ӧ�ġ�H= ���ú�E1��E2�Ĵ���ʽ��ʾ����
��2����֪�Ȼ�ѧ����ʽ��H2(g)+![]() O2(g) === H2O(g) ��H=��241.8kJ•mol-1���÷�Ӧ�Ļ��Ϊ167.2 kJ•mol-1�����淴Ӧ�Ļ��Ϊ ��
O2(g) === H2O(g) ��H=��241.8kJ•mol-1���÷�Ӧ�Ļ��Ϊ167.2 kJ•mol-1�����淴Ӧ�Ļ��Ϊ ��
��3������ͬһ��Ӧ��ͼ������(II)��ʵ��(I)��ȣ���ܴ�ͣ�����ӵİٷ������࣬��Ӧ���ʼӿ죬����Ϊ����ܵ�ԭ���� ��
��4������NaOH��Һ�ζ�δ֪Ũ�ȵ�HAʱ�����в�������������HAŨ��ƫ����� ��
A��������ˮϴ����ƿ��δ�����װ����Һ
B���ζ�ǰ���ֵζ��ܵļ��첿�������ݣ��ζ�����ʧ
C��װNaOH�ļ�ʽ�ζ���δ�ñ���NaOH��Һ��ϴ
D���ζ�ǰ���ӣ��ζ����Ӷ���

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2012?�Ϸ�һģ���л���A��C10H20O2������������ζ����֪��
��2012?�Ϸ�һģ���л���A��C10H20O2������������ζ����֪��| Ũ���� |
| �� |
| Ũ���� |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
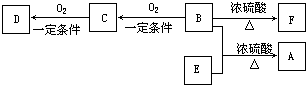
��14�֣��л���A��C10H20O2������������ζ��������������ϴ����ɵķ��㸳�����
��֪��
��B������û��֧����
��D����̼��������Һ��Ӧ�ų�������̼��
��D��E��Ϊ������ͬ�����ŵ�ͬ���칹�塣E���������ϵ�������Clȡ������һ�ȴ���ֻ��һ�֡�
��F����ʹ������Ȼ�̼��Һ��ɫ��
��1��B���Է����ķ�Ӧ�� ��ѡ����ţ���
��ȡ����Ӧ ����ȥ��Ӧ �ۼӾ۷�Ӧ ��������Ӧ
��2��D��F���������Ĺ����ŵ����������� �� ��
��3��д����D��E������ͬ�����ŵ�����ͬ���칹��Ľṹ��ʽ �� ��
��4����д��B+E��A�Ļ�ѧ��Ӧ����ʽ ��
��5��ijѧ������C�Ĺ�����ʱ��ȡ1mol/LCuSO4��Һ��2mol��LNaOH��Һ��lmL����һ֧�ྻ���Թ��ڻ�Ϻ��������ּ���0.5 mL 40����C�����Ⱥ���ɫ�������֡���ͬѧʵ��ʧ�ܵ�ԭ������� ����ѡ����ţ�
�ټ����C���� �ڼ����C̫��
�ۼ���CuSO4��Һ�������� �ܼ���CuSO4��Һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�꽭��ʡӥ̶�и����ڶ���ģ�⿼�����ۻ�ѧ���� ���ͣ������
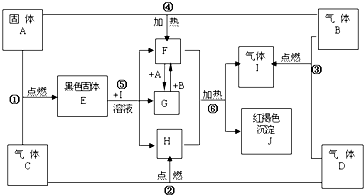
�������֣�����A��B��C��DΪ��ѧ�������ʣ������Ԫ�ص�ԭ���������μ�С��������ֻ�������Ƕ�����Ԫ�أ�BΪ����ɫ���塣�Ը�����ͼ�����ʵ��ת����ϵ�ش��������⡣
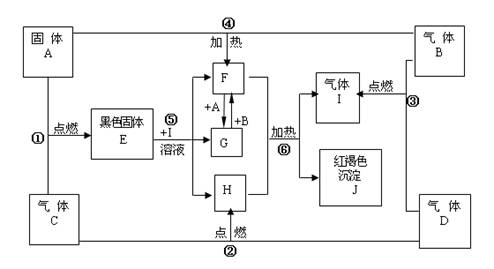
��1��A��_________
��2����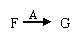 ��ת���У�A��������
���ڢ١��ķ�Ӧ�У�������������ԭ��Ӧ����
��������������֣�
��ת���У�A��������
���ڢ١��ķ�Ӧ�У�������������ԭ��Ӧ����
��������������֣�
��3��д��A�ڸ�������H��Ӧ�Ļ�ѧ��Ӧ����ʽ���������ת�Ƶķ������Ŀ
���������� ��
��4��д����Ӧ�Ļ�ѧ��Ӧ����ʽ���������� ��
��5����֪��101 kPa �����£�2 mol D��ȫȼ������Һ̬������ų����������� kJ����������д��ʾDȼ���ȵ��Ȼ�ѧ����ʽ�� ����������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com