
��16�֣������ͷ�ˮ���ؽ���Ԫ�ظ��Ķ��ԣ��ɽ�Cr2O72-ת��ΪCr(OH)3������ȥ�����ֽ����������ɳ�����pH���ұ���
| | ��ʼ������pH | ��ȫ������pH |
| Fe(OH)2 | 7.0 | 9.0 |
| Fe(OH)3 | 1.9 | 3.2 |
| Cr(OH)3 | 6.0 | 8.0 |


��1����8�֣���Al3++3H2O Al(OH)3+3H+��2�֣�
Al(OH)3+3H+��2�֣�
�� 1 Cr2O72-+ 3 HSO3-+ 5H+ = 2 Cr3++ 3 SO42-+ 4 H2O��2�֡�д��H+1�֣�ϵ����ȷ1�֣�
��Cr3++ 3OH-��Cr(OH)3����2�֣�ȡ��������ϲ���Һ�ⶨ��pH��1�֣�����pH��8���������ȫ��1�֣� ��2����8�֣���Cr2O72-+6Fe2++14H+��2Cr3++6Fe3++7H2O��3�֣�
��ˮ�е�H+���������ŵ磨1�֣���H+Ũ�ȼ�С��ʹˮ�ĵ���ƽ��H2O H++OH-�����ƶ���1�֣���������OH-Ũ���������������������������϶�������ȫ��1�֣� ��0.08��2�֡�˵�����������������������������
H++OH-�����ƶ���1�֣���������OH-Ũ���������������������������϶�������ȫ��1�֣� ��0.08��2�֡�˵�����������������������������
���������������1������������ˮ�������������ˮ��������������������������ԣ�������Ϊ��ˮ������Ӧ�����ӷ���ʽΪAl3++3H2O Al(OH)3+3H+��
Al(OH)3+3H+��
�ڸ��ݷ���ʽ��֪��Ԫ�صĻ��ϼ۴�+6�۽��͵�+3�۵õ�3�����ӣ���Ԫ�صĻ��ϼ۴�+4�����ߵ�+6��ʧȥ2�����ӣ����Ը��ݵ��ӵ�ʧ�غ��֪�������뻹ԭ�������ʵ���֮����1:3������ԭ���غ��֪��Ӧǰ���������Ӳμӣ���˷�Ӧ��ķ���ʽΪ1 Cr2O72-+ 3 HSO3-+ 5H+ = 2 Cr3++ 3 SO42-+ 4 H2O��
����Һ�к���Cr3+�������������ƺ���������������������Ӧ�����ӷ���ʽΪCr3++ 3OH-��Cr(OH)3��������������ȫ����ʱ��pH��Լ��8�����֤��Cr3+������ȫ�ķ�����ȡ��������ϲ���Һ�ⶨ��pH��1�֣�����pH��8���������ȫ��
��2����Cr2O72-����ǿ�������ܰ����������������������ӣ�����������ԭΪCr3+�����ݵ��ӵ�ʧ�غ��Լ�ԭ���غ��֪��Ӧ�ķ���ʽΪCr2O72-+6Fe2++14H+��2Cr3++6Fe3++7H2O��
��ˮ�е�H+���������ŵ�����������H+Ũ�ȼ�С��ʹˮ�ĵ���ƽ��H2O H++OH-�����ƶ���������OH-Ũ���������������������������϶�������ȫ��
H++OH-�����ƶ���������OH-Ũ���������������������������϶�������ȫ��
��1mol Cr2O72-�ڷ�Ӧ�еõ�6mol���ӣ�����������ʧȥ1�����ӣ���������Һ�к���0.01mol Cr2O72-�����������0.06mol�����ӣ�ͬʱ������0.02mol Cr3+�����������ȫ�����ɳ��������ʵ�����0.06mol+0.02mol��0.08mol��
���㣺����������ˮ��������ԭ��Ӧ��Ӧ���Լ��绯ѧԭ����Ӧ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�Ķ����в��Ϻ�ش����⡣
һ������60 kg�����ij����ˣ�����Լ����4 g������4 g���������ڲ����Ե��ʵ���ʽ���ڣ�������Fe2����Fe3������ʽ���ڡ��������������ױ����գ���ƶѪ�߲�����ʱ��Ӧ���躬Fe2���������Σ�����������������ά����C����ʹʳ���е�Fe3��ת��ΪFe2�����������������ա�
��1���������н���Fe2��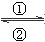 Fe3����ת��ʱ�� ���е�Fe2����________�������е�Fe3����___________����
Fe3����ת��ʱ�� ���е�Fe2����________�������е�Fe3����___________����
��2��������ά����C����ʹʳ���е�Fe3��ת��ΪFe2������仰ָ����ά����C����һ��Ӧ����___________��������___________�ԡ�
��3���г����۵�ij����Ƭ�к������Ŀ���ϸС�Ļ�ԭ���ۣ���Щ����������θ�ᣨ��Ҫ�ɷ������ᣩ��������ת���������Ρ��˷�Ӧ�����ӷ���ʽΪ_______________
�����õ����ŷ������ʽ�еĵ���ת�Ʒ������Ŀ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ϸ�Ķ�������������
����ϡ������Ԫ��Xe��믣�����Ԫ���γɵ�һ�ֹ��ۻ�����XeO3�����ȶ�����ת��Ϊ���ʶ���ǿ�����ԡ���������XeO3Ͷ�뺬Mn2+��ˮ��Һ�У���Һ��Ϊ�Ϻ�ɫ��pH���ϼ�С��
�ڽ�0.08 mol KMnO4���壨����Ϊ12.64 g������һ��ʱ����ռ���a mol O2����Ӧ������Ĺ����м���������Ũ���ᣬ���ռ���b mol Cl2����ʱMnԪ��ȫ����Mn2+����ʽ��������Һ�С�
��������ԭ��Ӧ��ʵ���ϰ��������ͻ�ԭ�������̡�������һ����ԭ���̵ķ�Ӧʽ��Cl2+2e- ��2Cl- ��
�ش����⣺
��1����д�����йص����ӷ���ʽ��________________________________________________��
��2������ƽ�ڵĻ�ѧ����ʽ��
____KMnO4+____HCl ��______KCl+ _____MnCl2+_____Cl2��+____ H2O
ͨ���Եڢڶ��������ṩ�����ݽ��м���ɵó���a +b�����ֵΪ ____ ��a +b��СֵΪ_____��
��3������������������ʹ���еĻ�ԭ���̷�����������________��
| A��Na2CO3 | B��KMnO4 | C��XeO3 | D��Na2SO3 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪Ca3(PO4)2��SiO2��C���¹��ȿ��Է�Ӧ�õ�CaSiO3��P4������CO�����������գ�
��1���÷�Ӧ����������_________������������_________��
��2��д���÷�Ӧ�Ļ�ѧ����ʽ____________________________________________��
��3��ÿ����24.0g̼ʱ���� mol���ӷ���ת�ƣ�����P4_______g��
��4����Ӧ���û�����壬����ɱ���£��������ܶ�Ϊ g/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ŷ��ԭ����2012��1��1�������պ���̼��˰��Ӧ�Ա����ڻ���ȫ����ӣ��о�̼���仯������ۺ����öԴٽ���̼���Ĺ���������Ҫ�����塣���������֪ʶ�о�̼���仯��������ʡ�
��1�����������ҹ���������̼���о�ȡ���ش��չ���õ绡���ϳɵ�̼�����г����д���̼������������)������̼���������������������ᴿ���䷴Ӧ�Ļ�ѧ����ʽΪ��
___C+___K2Cr2O7+___��___CO2��+ ___K2SO4+ ___Cr2(SO4)3+___H2O
����ɲ���ƽ������ѧ����ʽ��
������������ʽ�ϱ���÷�Ӧ����ת�Ƶķ�������Ŀ��
��2������ʱ����CO��ԭMgSO4���Ʊ��ߴ�MgO��
��750��ʱ����������к������ʵ���SO2��SO3����ʱ��Ӧ�Ļ�ѧ����ʽ________
����MgO���Ƴɡ�þ���������Ρ�ȼ�ϵ�أ���װ��ʾ��ͼ��ͼ1���õ�ط�Ӧ�����ӷ���ʽΪ_____________________��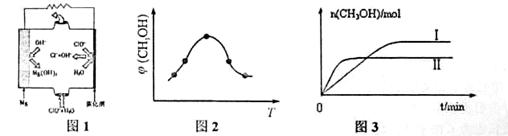
��3��������̼�ϳɼ״���̼���ŵ��·���CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ��
CO2(g)+3H2(g)��g�� CH3OH(g)+H2O(g) ��H
CH3OH(g)+H2O(g) ��H
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪK_______��
��ȡ��ݵ����CO2��H2�Ļ�����壨���ʵ���֮�Ⱦ�Ϊ1��3)���ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�����������Ӧ����Ӧ��ͬʱ���ü״����������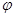 (CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ2��ʾ��������CO2ת��Ϊ�״���Ӧ�� ��H_____0 (�>������<���� =�� )��
(CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ2��ʾ��������CO2ת��Ϊ�״���Ӧ�� ��H_____0 (�>������<���� =�� )��
����ͬ�����·�����Ӧ�����CH3OH�����ʵ�����ʱ��仯��ͼ3��ʾ������ I��II��Ӧ��ƽ�ⳣ����С��ϵΪKI_______KII(�>������<���� = ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�ҹ��Ǹ��������,���������������һλ,��¯��������Ϊ�ձ������������ij�ֿ�ʯ����Ԫ����������FemOn����ʽ����,�ֽ�������ʵ��:����������ʯ��Ʒ����,��ȡ25.0 g��Ʒ���ձ���,����ϡ�������ܽ�,�����ϼ��ȡ�����,��ȥ�������������Һ�м���10.0 gͭ�۳�ַ�Ӧ����ˡ�ϴ�ӡ������ʣ�����3.6 g��ʣ����Һ��2 mol��L-1������KMnO4�ζ�,���յ�ʱ����KMnO4��Һ���25.0 mL��
(1)���������ʯ����Ԫ�ص�����������
(2)����������FemOn�Ļ�ѧʽ(m��nΪ������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
����̼ѭ����������������ĸ߶ȹ�ע������ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������������ȫ������ձ����ӡ�
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ƽ�÷�Ӧ�Ļ�ѧ����ʽ��������ѧ��������˳�����ڴ�����ϣ�
___C��____KMnO4��____H2SO4��___CO2����____MnSO4��____K2SO4��___H2O
��2������ͬ���CO��g����H2O��g���ֱ�ͨ�˵��ݻ�Ϊ2L�ĺ����ܱ������У��������·�Ӧ��
CO��g��+H2O��g�� CO2��g��+H2��g�� �õ�������������
CO2��g��+H2��g�� �õ�������������
| ʵ�� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
���������(Na2S2O3)�ɿ�����һ��Sԭ��ȡ����Na2SO4�е�һ��Oԭ�Ӷ��γɡ�ijУ��ѧ�о���ѧϰС���������ѧϰ��˼�룬ͨ��ʵ��̽��Na2S2O3�Ļ�ѧ���ʡ�����д���¿հ�:
��������⡿Na2S2O3�Ƿ���Na2SO4���ƾ߱����������أ�
����٣�________________________�� ����ڣ���Һ�����ԣ��Ҳ����ᷴӦ��
����ۣ���ԭ�ԣ����ܱ�������������
��ʵ��̽����������������ڡ��ۣ����ʵ�鷽��������д���б����еģ�1����2����3����
| | ʵ����� | ʵ������ ��Ԥ��ʵ������ | ������� �������ӷ���ʽ��ʾ�� |
| ����� | | ��ҺpHԼ8��10 | |
| ��pH=2�������еμ�Na2S2O3��Һ | | S2O32��+2H��=S��+SO2��+H2O | |
| ����� | ��������ˮ(pH<2)�еμ�����Na2S2O3��Һ | ��ˮ��ɫ��dz | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵���в���ȷ���� ( )
| A������з�̪��ˮ�м������Na2O2��ĩ������Һ����ɫ����ֱ���ɫ |
| B�������Na2O2��ĩ����֬���ϵμӼ���ˮ����֬����ȼ��������˵��Na2O2��H2O��Ӧ��һ�����ȷ�Ӧ������������ |
| C��Na2O2��H2O��Ӧ��һ��������ԭ��Ӧ��Na2O2���������������ǻ�ԭ�� |
| D��Na2O2��H2O��Ӧ��һ���û���Ӧ���е���O2���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com