
 CH3CH2OH(g)+3H2O(g).
CH3CH2OH(g)+3H2O(g).| CO2转化率(%) n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
 CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______.
CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______.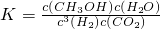 b.H2的平均反应速率为0.3mol/(L?s)
b.H2的平均反应速率为0.3mol/(L?s) 氧气”),b处电极上发生的电极反应是:______.
氧气”),b处电极上发生的电极反应是:______. (固体和纯溶剂不列入表达式)=
(固体和纯溶剂不列入表达式)=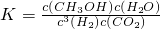 ,故a正确;
,故a正确;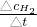 =0.3mol/(l?min),而不是3mol/(l?s),选项单位错误,故B错误;
=0.3mol/(l?min),而不是3mol/(l?s),选项单位错误,故B错误;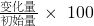 %=
%= ×100%=40%,故c错误;
×100%=40%,故c错误;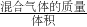 ,混合气体的质量遵循质量守恒,任何状态下质量均是定值,此反应又是在固定容积为2L的密闭容器中发生,所以体积在任何状态下均是定值,所以密度在任何状态下均是定值,故d错误,故答案为:bcd;
,混合气体的质量遵循质量守恒,任何状态下质量均是定值,此反应又是在固定容积为2L的密闭容器中发生,所以体积在任何状态下均是定值,所以密度在任何状态下均是定值,故d错误,故答案为:bcd;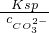 =
=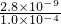 =2.8×10-5mo1/L,故答案为:2.8×10-5mo1/L.
=2.8×10-5mo1/L,故答案为:2.8×10-5mo1/L. (固体和纯溶剂不列入表达式中);
(固体和纯溶剂不列入表达式中);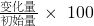 %,
%, ,看分子和分母的变化来判断是否为平衡状态;
,看分子和分母的变化来判断是否为平衡状态;

 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:单选题
 体积K2SO4溶液的试管
体积K2SO4溶液的试管查看答案和解析>>
科目:高中化学 来源: 题型:单选题
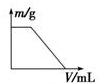
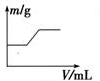
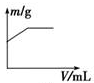

查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题




查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
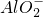 、
、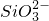 、
、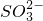 、
、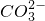 、
、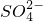 中的若干种离子.某同学对该溶液进行了如图所示实验:
中的若干种离子.某同学对该溶液进行了如图所示实验:
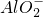 和
和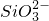 一定存在于溶液X中
一定存在于溶液X中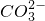 和
和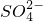 一定不存在于溶液X中
一定不存在于溶液X中查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com