
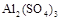 和
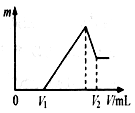
和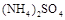 溶于水,形成VL混合溶液,向该混合溶液中逐滴加入某NaOH溶液直至过量。下列各图示中,能正确表示加入NaOH溶液的体积(x)与生成沉淀的物质的量(Y)的关系的是
溶于水,形成VL混合溶液,向该混合溶液中逐滴加入某NaOH溶液直至过量。下列各图示中,能正确表示加入NaOH溶液的体积(x)与生成沉淀的物质的量(Y)的关系的是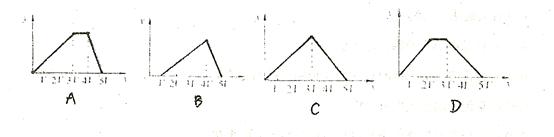
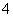 与Al3+结合OH-的能力:若NH
与Al3+结合OH-的能力:若NH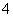 先与OH-结合,则生成的NH3·H2O还是能与Al3+结合释放出NH
先与OH-结合,则生成的NH3·H2O还是能与Al3+结合释放出NH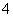 ,故结合OH-的顺序为:先Al3+,后NH
,故结合OH-的顺序为:先Al3+,后NH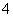 。再分析Al(OH)3与NH
。再分析Al(OH)3与NH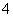 结合OH-的能力:若Al(OH)3先与OH-结合,则生成的AlO
结合OH-的能力:若Al(OH)3先与OH-结合,则生成的AlO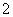 会与NH
会与NH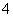 发生双水解反应:NH
发生双水解反应:NH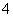 +AlO
+AlO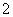 +H2O===Al(OH)3↓+NH3↑,又生成Al(OH)3沉淀,故结合OH-的顺序为:先NH
+H2O===Al(OH)3↓+NH3↑,又生成Al(OH)3沉淀,故结合OH-的顺序为:先NH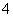 ,后Al(OH)3。当NH
,后Al(OH)3。当NH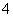 完全变为NH3·H2O后,随NaOH溶液的加入,Al(OH)3沉淀开始溶解至全部消失。因此各阶段反应的顺序为①Al3++3OH-===Al(OH)3↓,②NH
完全变为NH3·H2O后,随NaOH溶液的加入,Al(OH)3沉淀开始溶解至全部消失。因此各阶段反应的顺序为①Al3++3OH-===Al(OH)3↓,②NH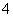 +OH-===NH3·H2O,③Al(OH)3+OH-===AlO
+OH-===NH3·H2O,③Al(OH)3+OH-===AlO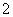 +2H2O。并注意生成Al(OH)3沉淀与沉淀溶解,消耗NaOH的体积比为3∶1。答案:A
+2H2O。并注意生成Al(OH)3沉淀与沉淀溶解,消耗NaOH的体积比为3∶1。答案:A

科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3: 2 | B.2:7 | C.1:4 | D.1:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
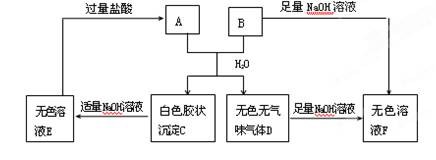
 离子方程式_________________________________________________________。
离子方程式_________________________________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
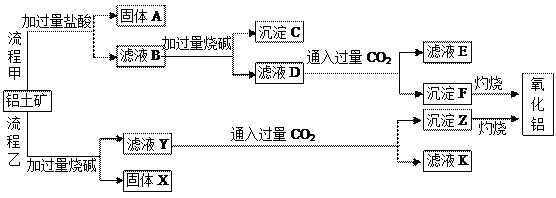
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.92g | B.0.2g | C.0.4g | D.无法求得 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com