
| A. | NaHCO3溶液中:c(H+)+c(H2CO3)=2c(CO32-)+c(OH-) | |
| B. | 向0.1 mol•L-1的NH4Cl溶液中通入一定量的NH3后:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | 向CH3COOH溶液中滴加NaOH使pH>7溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 0.3 mol•L-1的 HY溶液与0.3 mol•L-1的NaOH溶液等体积混合后所得pH=9的溶液中:c(OH-)-c(HY)=c(H+)=1×10-9 mol•L-1 |
分析 A.根据质子守恒分析;
B.根据电荷守恒分析;
C.当少量的CH3COOH与NaOH反应生成CH3COONa,溶液中NaOH的物质的量可能大于CH3COONa;
D.取0.3mol•L-1HY溶液与0.3mol•L-1NaOH溶液等体积混合,恰好生成NaY,测得混合溶液的pH=9,说明溶液呈碱性,NaY为强碱弱酸盐,结合电荷守恒和物料守恒分析.
解答 解:A.NaHCO3溶液中,存在质子守恒,即:c(H+)+c(H2CO3)=c(CO32-)+c(OH-),故A错误;
B.向0.1 mol•L-1的NH4Cl溶液中通入一定量的NH3后,电荷守恒为c(Cl-)+c(OH-)=c(H+)+c(NH4+),当c(Cl-)>c(NH4+)时,c(OH-)<c(H+),故B错误;
C.当少量的CH3COOH与NaOH反应生成CH3COONa,溶液中NaOH的物质的量可能大于CH3COONa,所以溶液中可能存在:c(Na+)>c(OH-)>c(CH3COO-)>c(H+),故C错误;
D.取0.3mol•L-1HY溶液与0.3mol•L-1NaOH溶液等体积混合,恰好生成NaY,测得混合溶液的pH=9,根据物料守恒,应有c(HY)+c(Y-)=c(Na+),根据电荷守恒应有c(Na+)+c(H+)=c(Y-)+c(OH-),二者联式可得:c(HY)+c(H+)=c(OH-),则c(OH-)-c(HY)=c(H+)=1×10-9mol•L-1,故D正确.
故选D.
点评 本题考查酸碱混合的定性判断以及离子浓度大小比较问题,注意根据题中信息判断盐类水解的特点,结合守恒思想解答该题,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2015年诺贝尔化学奖颁给了研究细胞修复自身DNA机制的三位科学家.DNA属于有机高分子,化学家鲍林(L.Pauling)提出的氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础 | |
| B. | 生物炼铜是指铜矿石在细菌作用下可把不溶性的硫化铜转化为可溶性铜盐,使铜的冶炼变得简单 | |
| C. | 埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液、双氧水均可以将病毒氧化而达到消毒的目的 | |
| D. | 扫描隧道显微技术、超分辨荧光显微技术等的发展促进了人类对微观结构的探索,可实现对原子或分子的操控,使科学研究迈入更高的水平层次 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
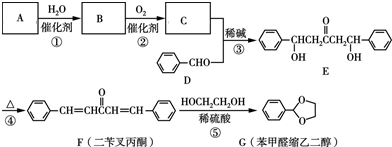
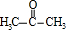 +2
+2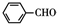 $\stackrel{碱}{→}$
$\stackrel{碱}{→}$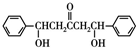 .
.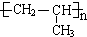 .
.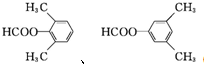 .
.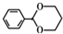 (无机物任选).
(无机物任选).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg$→_{点燃}^{CO_{2}}$C$→_{△}^{H_{2}SO_{4}(浓)}$SO3 | |
| B. | 0.1mol•L-1HCl$→_{△}^{MnO_{2}}$Cl2$\stackrel{石灰水}{→}$Ca(ClO)2(aq) | |
| C. | NaCl饱和溶液$\stackrel{NH_{3}、CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| D. | 淀粉溶液$→_{△}^{稀硫酸}$葡萄糖$→_{△}^{Cu(OH)_{2}悬浊液}$Cu2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
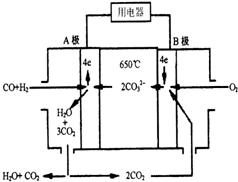 现有一个碳酸盐燃料电池,以一定比例的Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,直接以水煤气(CO、H2的体积比为1:1)为燃料,其工作原理如图所示.
现有一个碳酸盐燃料电池,以一定比例的Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,直接以水煤气(CO、H2的体积比为1:1)为燃料,其工作原理如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 石油的分馏、煤的干馏均是物理变化 | |
| B. | 应当大力实施矿物燃料“脱硫“、脱硝技术”,减少硫的氧化物和氮氧化物的污染 | |
| C. | 近期我国华北地区出现雾霸天气,PM2.5超标.PM2.5仅来自煤的燃烧 | |
| D. | 根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在中和滴定实验中,锥形瓶须用待测液润洗 | |
| B. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| C. | 用标准盐酸溶液滴定未知浓度NaOH溶液时,若滴定前滴定管尖嘴处有气泡未排出而滴定后消失,则能使所测结果偏高 | |
| D. | 滴定时可将KMnO4溶液装在碱式滴定管中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
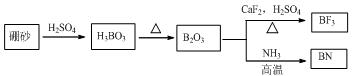
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com