
【题目】甲、乙、丙均为化合物,其中甲为淡黄色的固体,乙常温下为无色无味液体,丙为常见的无色无味气体。它们有如下图的转化关系,已知D为黄绿色气体,按要求回答下列问题:

(1)甲物质为_____________(填化学式)。
(2)1mol乙和足量甲反应可生成______________mol B物质;1mol丙和足量甲反应可生成____________mol B物质。
(3)D能使湿润的有色布条褪色,其褪色原因是_______________。(结合化学反应方程式描述原因)
(4)丙与溶液F反应的化学方程式为_____________________。
【答案】(1)Na2O2;(2)0.5;0.5;
(3)Cl2+H2O![]() HCl+HClO ,HClO有强氧化性,能将有色物质氧化为无色物质,而使布条褪色
HCl+HClO ,HClO有强氧化性,能将有色物质氧化为无色物质,而使布条褪色
(4)CO2+NaClO+H2O=NaHCO3+HClO。
【解析】
试题分析:甲、乙、丙均为化合物,甲为淡黄色的固体,乙常温下为无色无味液体,丙为常见的无色无味气体,甲能既能与乙反应也能与丙反应,可知甲为Na2O2,乙为H2O,丙为CO2,则A为NaOH,B为O2,C为Na2CO3。D为黄绿色气体,则D为Cl2,D(氯气)与A(氢氧化钠)反应生成NaCl、NaClO,F能与丙(二氧化碳)反应C与I,则F为HClO、E为NaCl、I为NaHCO3。G与C(碳酸钠)反应得到E(氯化钠)与丙(二氧化碳),则G为HCl。(1)由上述判断可知,甲物质为Na2O2;(2)乙与足量的甲发生反应:2Na2O2+2H2O=4NaOH+O2↑,1mol水反应可以生成0.5mol氧气,丙和足量甲发生反应:2Na2O2+2CO2 =2Na2CO3+ O2,1mol二氧化碳反应生成0.5mol氧气;(3)D(氯气)能使湿润的有色布条褪色,其褪色原因是:溶于水反应产生HCl和HClO,Cl2+H2O![]() HCl+HClO ,HClO有强氧化性,能将有色物质氧化为无色物质,而使布条褪色;(4)由于酸性H2CO3>HClO,所以丙与溶液F反应是二氧化碳与次氯酸钠反应生成碳酸氢钠与HClO,反应的化学方程式为:CO2+NaClO+H2O=NaHCO3+HClO。
HCl+HClO ,HClO有强氧化性,能将有色物质氧化为无色物质,而使布条褪色;(4)由于酸性H2CO3>HClO,所以丙与溶液F反应是二氧化碳与次氯酸钠反应生成碳酸氢钠与HClO,反应的化学方程式为:CO2+NaClO+H2O=NaHCO3+HClO。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)![]() pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )

①m+n>p
②x点表示的正反应速率大于逆反应速率
③n>p
④x点比y点时的反应速率慢
⑤若升高温度,该反应的平衡常数增大.
A.①②⑤ B.只有②④ C.只有①③ D.只有①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有下列6种离子中的某几种:Cl-、SO42-、CO32-、NH4+ 、Na+、K+。 为确认溶液组成进行如下实验:
(1)取200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。
(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,已知加热时:NH4++OH-=NH3↑+H2O,假定产生的气体全部逸出).由此可以推断原溶液组成
(1)一定存在____________可能存在______________
(2)c(CO32-)=_______________________
(3)如果上述6种离子都存在,则c(Cl-)________c(SO42-)(填>、=、<)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶液中,一定能大量共存的是

A. a点对应的溶液中:Na+、OH-、SO42-、NO3-
B. b点对应的溶液中:Al3+、Fe3+,MnO4-、Cl-
C. c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D. d点对应的溶液中:F-、NO3-、Fe2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气体由常见的一种或多种气体组成,经测定其中只含有碳、氧两种元素,碳、氧元素的质量比为3:8,则关于该气体的说法正确的( )是
A.该气体一定是纯净物
B.该气体一定是CO、CO2的混合物
C.该气体中所含的物质最多只有2种
D.该气体可能含有3种成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为VL的密闭容器中进行反应:aN(g)bM(g),M、N的物质的量随时间的变化曲线如下图示。

(1)此反应的化学方程式中a:b =
(2)t1到t2时刻,以M的浓度变化表示的平均化学反应速率为
(3)此反应在该条件下达到限度时,反应物的转化率为
(4)下列叙述中能说明上述反应达到平衡状态的是
A.反应中M与N的物质的量之比为1:1 |
B.混合气体的总质量不随时间的变化而变化 |
C.混合气体的总物质的量不随时间的变化而变化 |
D.单位时间内消耗amol N ,同时生成bmol M |
E.混合气体的压强不随时间的变化而变化
F.N的转化率达到最大,且保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知二羟甲戊酸(如图)是生物合成青蒿素的原料之一。下列关于二羟甲戊酸的说法正确的是( )
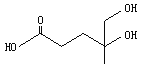
A.二羟甲戊酸的分子式为C6H10O4
B.1mol二羟甲戊酸与足量的Na钠反应生成1mol H2
C.二羟甲戊酸与乙醇、乙酸均能发生酯化反应
D.二羟甲戊酸不能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国及美国、日本等国家都已研制出了一种陶瓷柴油机,这种柴油机的发动机部件的受热面是用一种耐高温且不易传热的材料来制造的,这种材料是:
A. 普通硅酸盐陶瓷 B. 氮化硅陶瓷 C. 光导纤维 D. 玻璃钢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】南北朝时期炼丹家陶弘景在《陶隐居集》中记载了某种物质的鉴定分析法:“先时有人得一种物,其色理与芒硝大同小异,外观如雪,强烧之,紫青烟起,仍成灰,云是真硝石也。”这种物质是 ( )
A. KNO3 B. CuSO4·5H2O C. KMnO4 D. Na2SO4·10H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com