

人工吹制玻璃器皿
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:058
根据CO还原铁的氧化物的实验装置图(如下图所示),回答下列问题:
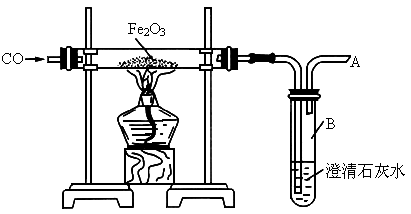
(1)怎样知道硬质玻璃管中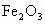 已开始反应?
已开始反应?
_________________________________________
(2)在A处点燃,可观察到什么现象?为什么要点燃
__________________________________________
(3)实验结束时应注意的操作是
___________________________________________
①先停止通入CO;②先熄灭酒精灯,并继续通入CO;③熄灭酒精灯,同时停止通入CO;④先熄灭酒精灯,继续通入CO至被还原的铁粉冷却,并点燃排出的CO气体
(4)现有铁的某种氧化物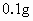 ,被CO完全还原后,在B中可过滤得到
,被CO完全还原后,在B中可过滤得到 固体物质(已知石灰水过量),则铁的氧化物的化学式是_______
固体物质(已知石灰水过量),则铁的氧化物的化学式是_______
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
根据CO还原铁的氧化物的实验装置图(如下图所示),回答下列问题:

(1)怎样知道硬质玻璃管中 已开始反应?
已开始反应?
_________________________________________
(2)在A处点燃,可观察到什么现象?为什么要点燃
__________________________________________
(3)实验结束时应注意的操作是
___________________________________________
①先停止通入CO;②先熄灭酒精灯,并继续通入CO;③熄灭酒精灯,同时停止通入CO;④先熄灭酒精灯,继续通入CO至被还原的铁粉冷却,并点燃排出的CO气体
(4)现有铁的某种氧化物 ,被CO完全还原后,在B中可过滤得到
,被CO完全还原后,在B中可过滤得到 固体物质(已知石灰水过量),则铁的氧化物的化学式是_______
固体物质(已知石灰水过量),则铁的氧化物的化学式是_______
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)烧杯间填满碎泡沫塑料的作用是__________________;
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替?______(填“能”或“不能”),其原因是___________________________________;

(3)为什么氢氧化钠溶液的浓度要用0.55 mol·L-1?___________________________;
实验中若改用60 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”“不相等”),若实验操作均正确,则所求中和热_________(填“相等”“不相等”);
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:_____________________________;
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得的结果偏低,请你分析结果偏低的原因可能是_________(填字母代号)。
a.测量盐酸的温度后,温度计没有用水冲洗干净
b.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
c.做本实验的当天室温较高
d.将50 mL 0.55 mol·L-1的氢氧化钠溶液取成了50 mL 0.55 mol·L-1的氨水
e.在量取盐酸时仰视读数
f.大烧杯的盖板中间小孔太大
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)怎样知道硬质玻璃管中Fe2O3已开始反应?__________________________________。
(2)在A处点燃,可观察到什么现象?为什么要点燃?___________________________。
(3)实验结束时应注意的操作是_________。
①先停止通入CO
②先熄灭酒精灯,并继续通入CO
③熄灭酒精灯,同时停止通入CO
④先熄灭酒精灯,继续通入CO至被还原的铁粉冷却,并点燃排出的CO气体
(4)现有铁的某种氧化物0.1 g,被CO完全还原后,在B中可过滤得到0.172 4 g固体物质(已知石灰水过量),则铁的氧化物的化学式是 ____________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
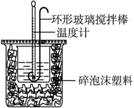
用50 mL 0.50 mol · L-1的盐酸与50 mL 0.55 mol · Lf-1的氢氧化钠溶液在如下图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。完成下列问题:
(1)烧杯间填满碎泡沫塑料的作用是__________________;
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替?______(填“能”或“不能”),其原因是___________________________________;
(3)为什么氢氧化钠溶液的浓度要用0.55 mol · L-1?___________________________;
实验中若改用60 mL 0.50 mol · L-1的盐酸与50 mL 0.55 mol · L-1的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”“不相等”),若实验操作均正确,则所求中和热_________(填“相等”“不相等”);
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:_____________________________;
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得的结果偏低,请你分析结果偏低的原因可能是_________(填字母代号)。
a.测量盐酸的温度后,温度计没有用水冲洗干净
b.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
c.做本实验的当天室温较高
d.将50 mL 0.55 mol · L-1的氢氧化钠溶液取成了50 mL 0.55 mol · L-1的氨水
e.在量取盐酸时仰视读数
f.大烧杯的盖板中间小孔太大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com