
ij��ѧ��Ӧ2A B+D�����ֲ�ͬ�����½��У�B��D��ʼŨ��Ϊ0����Ӧ��A��Ũ��(mol ��L-1)�淴Ӧʱ��(min)�ı仯������±���ʾ��
B+D�����ֲ�ͬ�����½��У�B��D��ʼŨ��Ϊ0����Ӧ��A��Ũ��(mol ��L-1)�淴Ӧʱ��(min)�ı仯������±���ʾ��
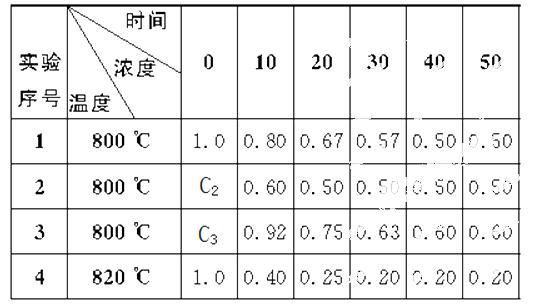
�����������ݣ����������գ�
(1)��ʵ��1�У���Ӧ��10��20 minʱ����ƽ����Ӧ����Ϊ________mol ��L-1��min-1��
(2)��ʵ��2�У�A�ij�ʼŨ��c2=________mol ��L-1����Ӧ��20 min�ʹﵽƽ�⣬���Ʋ�ʵ��2�л�������������_______________________ _____��
(3)��ʵ��3�ķ�Ӧ����Ϊv3��ʵ��1�ķ�Ӧ����Ϊv1����v3____v1(�������=������)����c3____1.0 mol ��L-1(�������=������)��
(4)��ʵ��4�У���Ӧ��20��30 minʱ����ƽ����Ӧ����Ϊ________��
�Ƚ�ʵ��4��ʵ��1�����Ʋ�÷�Ӧ��_______(����ȡ����ȡ�)��Ӧ����ϱ�������˵��ԭ��______ _ _____��
 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ����Cl2��FeCl2��KSCN�����Һ�ķ�Ӧ����ʵ��̽����
| �� �� | �� �� |
| ͨ������������ | I��A����Һ��� |
��1��B�з�Ӧ�����ӷ���ʽ�� ��
��2��A����Һ����ԭ���� ��
��3��Ϊ��̽������II��ԭ��ͬѧ��������ʵ�顣
��ȡA�л�ɫ��Һ���Թ���,����NaOH��Һ,�к��ɫ�������ɣ�����Һ��һ������ ��
��ȡA�л�ɫ��Һ���Թ��У����������KSCN��Һ�����յõ���ɫ��Һ��
��ͬѧ��ʵ��֤����������II��ԭ����SCN����Cl2�����˷�Ӧ��
��4����ͬѧ����SCN�����ܱ�Cl2�����ˣ����ֽ����������о���
������ʾ��SCN���ĵ���ʽΪ 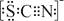 ��
��
�ټ�ͬѧ��ΪSCN����̼Ԫ��û�б������������� ��
��ȡA�л�ɫ��Һ���Թ��У������������ữ��BaCl2��Һ��������ɫ�������ɴ�֤��SCN���б�������Ԫ���� ��
��ͨ��ʵ��֤����SCN- �е�Ԫ��ת��ΪNO3-������ʵ�鷽���� ��
����SCN����Cl2��Ӧ����1 mol CO2����ת�Ƶ��ӵ����ʵ����� mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ȷ�Ϸ����˻�ѧƽ���ƶ�����(����)
A����ѧ��Ӧ���ʷ����˸ı�
B������̬���ʲμӵĿ��淴Ӧ�ﵽƽ��ı���ѹǿ
C������ijһ�����ĸı䣬ʹƽ�������и���ֵ�Ũ�ȷ����˲�ͬ�̶ȵĸı�
D�����淴Ӧ�ﵽƽ���ʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��0.6molX�����0.4molY���������ݻ�Ϊ2L�������У�ʹ�䷢�����·�Ӧ��3X(g)+Y(g)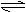
 nZ(g)+2W(g)��5minĩ����0.2molW������֪��ZŨ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.01mol/(L��min)������ֵΪ ( )
nZ(g)+2W(g)��5minĩ����0.2molW������֪��ZŨ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.01mol/(L��min)������ֵΪ ( )
����4 B��3 C��2 D��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
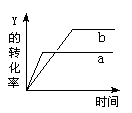
��Ӧ X(��)�� Y(��) 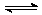 2Z(��)�� Q(Q��0),��һ�������£���Ӧ��Y��ת�����뷴Ӧʱ��(t)�Ĺ�ϵ����ͼ��ʾ����ʹ����a��Ϊ����b�ɲ�ȡ�Ĵ�ʩ��( )
2Z(��)�� Q(Q��0),��һ�������£���Ӧ��Y��ת�����뷴Ӧʱ��(t)�Ĺ�ϵ����ͼ��ʾ����ʹ����a��Ϊ����b�ɲ�ȡ�Ĵ�ʩ��( )
A.������� B.�����¶�
C.����ѹǿ D.����Y��Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����K2CO3��Ӧʱ����ʹ��Ӧ������������Լӿ���ǣ� ��
A.��������������һ�� B.�����Ũ������һ������������
C.�¶�����30 �� D.����K2CO3��ĩ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶Ⱥ�ѹǿ�£���1 molij����A���������·�Ӧ2A��g��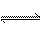 xB(g)+C(g)�����ﵽƽ��ʱ��A�ڻ�����е��������Ϊ58.84%,�������������Ϊ46 g,ƽ����Է�������Ϊ39.8,��
xB(g)+C(g)�����ﵽƽ��ʱ��A�ڻ�����е��������Ϊ58.84%,�������������Ϊ46 g,ƽ����Է�������Ϊ39.8,��
��1��A�ķֽ��ʣ�
��2��x��ֵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ͬ��ijֲ��Ӫ��Һ�����䷽���£�
|
����
��� | KCl | K2SO4 | ZnSO4 | ZnCl2 |
| �� | 0.3mol | 0.2mol | 0.1mol | �� |
| �� | 0.1mol | 0.3mol | �� | 0.1mol |
�٢�����Ӫ��Һ�ijɷ֣��������ӣ�:
A. ��n(K+)��ͬ B. ��n(Cl-)��ͬ C. ����ȫ��ͬ D. ��ȫ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ڻ�ѧ��Ӧ3W(g)��2X(g) ��4Y(g)��3Z(g)�����з�Ӧ���ʹ�ϵ����ȷ����
A��v(W)��3v(Z)�� B��2v(X)��3v(Z) C��2v(X)��v(Y) D��3v(W)��2v(X)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com