
| A、潮湿的氯气通过盛有浓H2SO4的洗气瓶 | ||||
| B、碳与浓H2SO4 加热反应 | ||||
| C、浓H2SO4使木条变黑 | ||||
D、实验室用浓H2SO4制HCl 其方程式:2NaCl+H2SO4(浓)
|
| ||


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
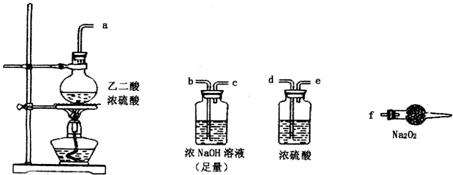
 有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:
有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有② | B、①和③ | C、①和④ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年吉林省高三上学期期初考试化学试卷 题型:填空题
(13分)甲是一种盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素。甲溶于水后可电离出三种离子,其中一种离子是由A、B两元素形成的10电子阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色;
③取少量甲溶液于试管中加入足量NaOH溶液,加热,部分实验现象如下:产生有刺激气味的气体;
④取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀。
回答下列问题:
(1)C的元素符号是 ,D在周期表中的位置: 周期 族
(2)用离子方程式表示实验②中现象的原因: 。
(3)实验③中出现的现象还有 。
(4)经测定甲晶体的摩尔质量为284 g/mol,其中阳离子与阴离子物质的量之比为3:2,则甲晶体的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
①准确称量3.920 g晶体溶于适量的稀硫酸中,配成100 mL浅绿色溶液X。
②取少量X于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色。
③取少量X于试管中加入浓NaOH溶液,加热,生成的气体能使湿润的红色石蕊试纸变蓝。
④取出20.00 mLX于锥形瓶中,用0.020 mol·L-1KMnO4溶液滴定(不需要指示剂),当到达终点时,用去KMnO4溶液20.00 mL。
⑤再取20.00 mLX加入足量浓NaOH溶液,加热,生成的气体恰好被20 mL0.10 mol·L-1 H2SO4溶液完全吸收(生成正盐)。
⑥另取20.00 mLX向其中加入足量的BaCl2溶液,将沉淀过滤、洗涤、烘干、称量得1.00 g。
(提示:酸性KMnO4被还原成Mn2+,Mn2+在稀溶液中几乎呈无色)
试回答下列有关问题:
(1)A中所含的阳离子是_________;所含的阴离子为_________。
(2)把A溶于稀硫酸而不直接溶于水的主要原因是__________________
(3)第④操作中,对滴定管的使用主要有以下几步:
a.用特制洗涤液洗涤;b.用自来水冲洗后,用蒸馏水洗涤;c.再用_________润洗两次;d.装入标准液后,_________;e.调节标准溶液的液面在“0”或“0”刻度以下,固定在滴定架上。
(4)此实验的名称_________。
(5)此方案设计中有一步操作失误(此步操作在实验中无意义),它是第_________ (填编号),此步实验应如何设计?
(6)如果通过实验测得3.920 g晶体中含有的阴离子全部形成钡盐沉淀的质量为4.66 g,则A的化学式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com