

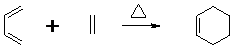
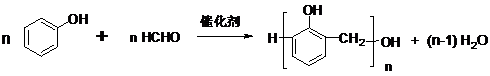
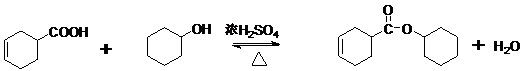
���� ��ϩ��NBS����ȡ����Ӧ����CH2=CHCH2Br��CH2=CHCH2Br����������ˮ��Һ�����������·���ˮ�ⷴӦ����CH2=CHCH2OH����B�Ľṹ�������Ϣ��֪XΪCH2=CHCH=CH2��B��������������CΪ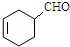 ��C��������Һ����������Ӧ����DΪ
��C��������Һ����������Ӧ����DΪ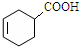 ��������E��һ�ֳ����ķ��㻯�������ʽΪC6H6O���� FeCl3��Һ����ɫ����EΪ
��������E��һ�ֳ����ķ��㻯�������ʽΪC6H6O���� FeCl3��Һ����ɫ����EΪ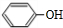 �����������������Ӧ����FΪ
�����������������Ӧ����FΪ ��F��D����������Ӧ����HΪ
��F��D����������Ӧ����HΪ ���������ȩ�������۷�Ӧ���ɸ߷��ӻ�����GΪ
���������ȩ�������۷�Ӧ���ɸ߷��ӻ�����GΪ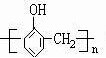 ��
��
��� �⣺��ϩ��NBS����ȡ����Ӧ����CH2=CHCH2Br��CH2=CHCH2Br����������ˮ��Һ�����������·���ˮ�ⷴӦ����CH2=CHCH2OH����B�Ľṹ�������Ϣ��֪XΪCH2=CHCH=CH2��B��������������CΪ ��C��������Һ����������Ӧ����DΪ
��C��������Һ����������Ӧ����DΪ ��������E��һ�ֳ����ķ��㻯�������ʽΪC6H6O���� FeCl3��Һ����ɫ����EΪ
��������E��һ�ֳ����ķ��㻯�������ʽΪC6H6O���� FeCl3��Һ����ɫ����EΪ �����������������Ӧ����FΪ
�����������������Ӧ����FΪ ��F��D����������Ӧ����HΪ
��F��D����������Ӧ����HΪ ���������ȩ�������۷�Ӧ���ɸ߷��ӻ�����GΪ
���������ȩ�������۷�Ӧ���ɸ߷��ӻ�����GΪ ��
��
��1��������CΪ ������ʽΪC7H10O�����������ŵ������ǣ�ȩ����̼̼˫����
������ʽΪC7H10O�����������ŵ������ǣ�ȩ����̼̼˫����
�ʴ�Ϊ��C7H10O��ȩ����̼̼˫����
��2����Ӧ1����±����ˮ�ⷴӦ���ɴ�����Ӧ�Լ��������ǣ�NaOHˮ��Һ�����ȣ�
�ʴ�Ϊ��NaOHˮ��Һ�����ȣ�
��3����Ӧ2�ķ�Ӧ�����ǣ��ӳɷ�Ӧ��XΪCH2=CHCH=CH2��������X�������ǣ�1��3-����ϩ��
�ʴ�Ϊ���ӳɷ�Ӧ�� 1��3-����ϩ��
��4����Ӧ3��E��G�ķ�Ӧ����ʽΪ��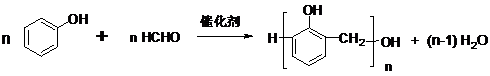 ��
��
��Ӧ4��D+F��H�ķ�Ӧ����ʽΪ��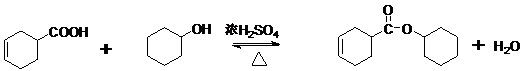 ��
��
�ʴ�Ϊ��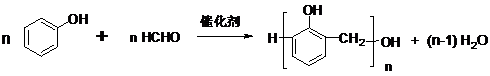 ��
��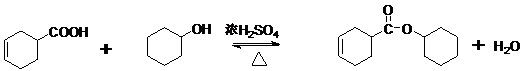 ��
��
��5��������B�ж���ͬ���칹�壬��������������������̼̼˫����������Ԫ���ڣ����������ǻ������ǻ�����ֱ����̼̼˫�����������������������칹����������ϩ��ȡ��������Ϊ-CH2OH����3�֣�����B����ȡ����Ϊ-CH3��-OH��-CH3ȡ��˫����Hԭ��ʱ��-OH��4��λ�ã�-CH3ȡ��˫����λ̼ԭ���ϵ�Hԭ��ʱ��-OH��4��λ�ã�-CH3ȡ��˫����λ̼ԭ���ϵ�Hԭ��ʱ��-OH��4��λ�ã��ʲ�����B���ڹ���14�֣�
�ʴ�Ϊ��14��
���� ���⿼���л�����ƶ���ϳɣ���������л���Ľṹ�����ƶϣ����ؿ���ѧ����ѧ�����������������չ����ŵ�������ת������5����ע���ж�ȡ���������ö�һ��һ���ж϶�Ԫȡ��ͬ���칹�壮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.01mol•L-1��H2SO4��Һ | B�� | 0.01mol•L-1��Ba��OH��2��Һ | ||
| C�� | c��OH-��=1��10-11mol•L-1����Һ | D�� | c��H+��=1��10-12mol•L-1����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
 ��0.1mol•L-1NaOH��Һ�ζ�10mL0.1mol•L-1H2A��Һ����Һ��pH��NaOH��Һ�������ϵ��ͼ��ʾ������˵��������ǣ�������
��0.1mol•L-1NaOH��Һ�ζ�10mL0.1mol•L-1H2A��Һ����Һ��pH��NaOH��Һ�������ϵ��ͼ��ʾ������˵��������ǣ�������| A�� | A����Һ�м�������ˮ��$\frac{c��O{H}^{-}��}{c��{H}_{2}A��}$���� | |
| B�� | B�㣺c��Na+����c��HA-����c��H+����c��A2-����c��OH-�� | |
| C�� | C�㣺c��Na+��=c��HA-��+2c��OH-�� | |
| D�� | ˮ���������c��OH-����B��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
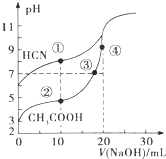
| A�� | �����Һ�У�c��OH-��=c��H+��+c��CH3COOH�� | |
| B�� | �����Һ��c��CN-���������Һ��c��CH3COO-�� | |
| C�� | �����Һ�У�c��Na+����c��CH3COO-����c��OH-����c��H+�� | |
| D�� | �ڵ�ں͢�֮�䣨�������˵㣩��������Ũ�ȴ�С��ϵ��c��CH3COO-����c��Na+����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
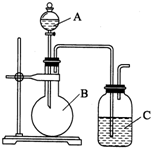 ijͬѧ�����ͼװ�ã�̽���ǽ������ʱ仯���ɣ�
ijͬѧ�����ͼװ�ã�̽���ǽ������ʱ仯���ɣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
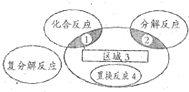
| A�� | Br2+SO2+2H2O�TH2SO4+2HBr | B�� | CuO+CO$\frac{\underline{\;\;��\;\;}}{\;}$Cu+CO2 | ||
| C�� | 4NH3+5O2�T4NO+6H2O | D�� | 3Fe+4H2O��g��$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����C������H2O��ת�������� | |
| B�� | ��С��������������淴Ӧ���ʾ���С | |
| C�� | ���������ƽ�ⳣ������ | |
| D�� | �����¶ȣ�ƽ�����淴Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com